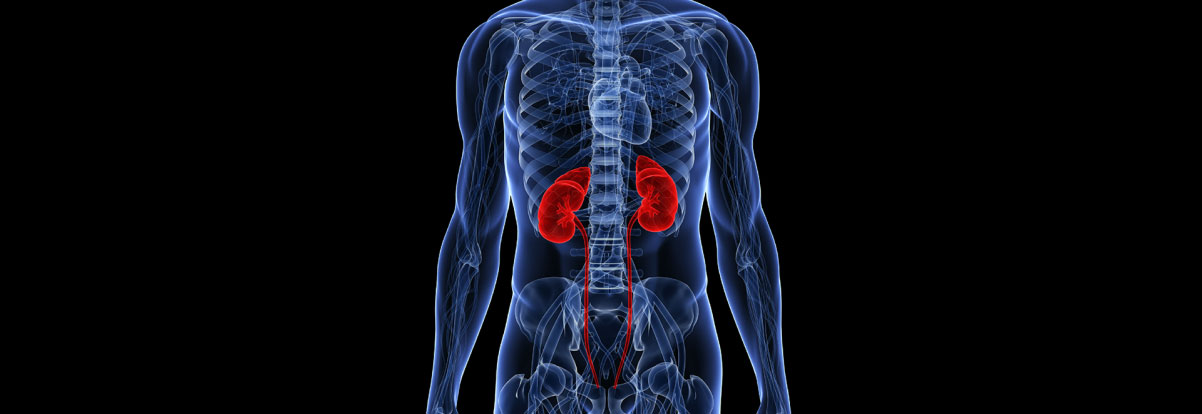
Atualmente, o câncer renal, representa cerca de 3% das doenças malignas em adultos no mundo. No Brasil, surgiu mais de 580 mil casos novos até o final de 2015, sendo duas vezes mais frequente nos homens que nas mulheres. O tipo mais comum do câncer renal é o carcinoma de células renais, que representa 90% dos casos, e se origina nos rins, podendo se espalhar pelo corpo. Dados publicados pelo Globocan, um projeto da Organização Mundial da Saúde que visa coletar, organizar e divulgar dados estimativos da incidência e mortalidade dos tipos mais comuns de câncer no mundo, apontam que, em 2015, 6.768 pessoas receberam o diagnóstico de câncer de rim no Brasil, sendo 4.068 homens e 2.700 mulheres. A maioria das pessoas com câncer renal são mais velhas. A idade média das pessoas quando diagnosticadas é de 65 anos. O câncer de rim é muito raro em pessoas com menos de 45 anos de idade. Ele está entre os 10 tipos de cânceres mais comuns em homens e mulheres. No geral, o risco de desenvolver câncer de rim é cerca de 1 em 63 (1,6%).
Sobre os Rins:
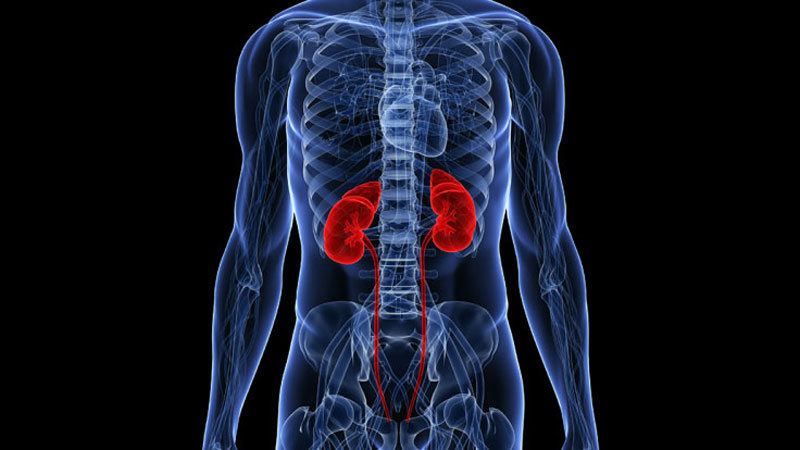
Os rins são um par de órgãos em formato de um feijão. Um rim está localizado do lado esquerdo e o outro do lado direito da coluna vertebral. Ambos estão protegidos pela caixa torácica. A principal função dos rins é filtrar o sangue e remover do corpo o excesso de água, sal e produtos residuais. Os produtos residuais filtrados são concentrados na urina. Os rins também ajudam a verificar se o corpo tem eritrócitos (também conhecidos como glóbulos vermelhos ou hemácias) suficientes. Os rins também atuam secretando substâncias importantes para nossa saúde. Entre suas funções, pode-se destacar a manutenção do equilíbrio de eletrólitos no corpo, como sódio, potássio, cálcio, magnésio, fósforo, bicarbonato etc.; a regulação do equilíbrio ácido-básico, mantendo o pH sanguíneo constante; a excreção de substâncias exógenas, como medicações; e a produção de hormônios, como aldosterona e prostaglandinas.
O câncer de rim é também conhecido como hipernefroma ou adenocarcinoma renal. Existem vários tipos de câncer renal. O mais frequente é o câncer renal de células claras, sendo responsável por 85% dos tumores diagnosticados. Entenda sobre o Câncer Renal de Células Claras: O CCR de célula clara é o tipo de célula associado com a mutação no gene von Hippel Lindau (VHL) no câncer renal hereditário. De fato, aproximadamente 70% dos casos não hereditários de CCR de células claras também apresentam mutação no aVHL.
Conheça os Tipos de Câncer Renal:
– Carcinoma de Células Renais (CCR)
Nem todos os cânceres renais são os mesmos. Há um crescente entendimento entre os médicos e pesquisadores de que há diferentes subtipos de CCR e que eles se comportam de formas completamente diferentes, tanto com relação ao quanto são agressivos no paciente quanto como eles respondem ao tratamento. Há dez ou quinze anos, era comum para um relato de patologia de um paciente com câncer renal se ler simplesmente Carcinoma de Células Renais. Hoje, este diagnóstico simples é considerado incompleto. A identificação do subtipo específico ou tipo de célula (histologia) do câncer renal pode ser tão importante na determinação do prognóstico do paciente quanto saber o estágio e o grau do CCR. Seu médico deve lhe oferecer informações sobre a histologia, grau e estágio do seu câncer renal. Em caso negativo, você deve se sentir confortável em pedir estas informações uma vez que é uma parte importante do seu planejamento de tratamento.
Os subtipos de CCR vêm da descrição da aparência das células e outras características. Eles incluem:
– Carcinoma de Células Renais (CCR) de Células Claras
Esta é a forma mais comum de câncer renal e representa entre 66% e 75% de todos os casos. O CCR de célula clara é o tipo de célula associado com a mutação no gene von Hippel Lindau (VHL) no câncer renal hereditário. De fato, aproximadamente 70% dos casos não hereditários de CCR de células claras também apresentam mutação no aVHL. Muito da pesquisa atual, que tenta identificar novos tratamentos efetivos para pacientes com doença localmente avançada ou metastática, foca neste subtipo da doença, uma vez que é o tipo mais comum de CCR.
Quando o tumor não está espalhado, o prognóstico é muito bom depois de excisão cirúrgica. O prognóstico para o paciente está diretamente relacionado tanto com o estágio (tamanho do tumor e faixa de crescimento) quanto o grau (as características das células tumorais) do câncer. Tanto o estágio quanto o grau são explicados mais adiante neste capítulo.
Pacientes com CCR de células claras metastático – ou um tumor que se espalhou para outras partes do corpo – apresentam um prognóstico significativamente mais desfavorável.
– Carcinoma de Células Renais (CCR) Papilar
Esta é a segunda forma mais comum de câncer renal, somando aproximadamente 15% dos casos.
O CCR papilar é dividido em dois subtipos com base na aparência celular: Tipo I (5%) e Tipo II (10%). Há um aumento na incidência de CCR papilar em afro-americanos e um aumento na incidência de doença bilateral (envolvendo ambos os rins) associado com este subtipo.
Há também formas hereditárias tanto do CCR papilar Tipo I quanto Tipo II. Quando o CCR papilar não está espalhado, a remoção cirúrgica está geralmente associada a um excelente prognóstico. No entanto, quando ocorre metástase do CCR papilar para outros locais do corpo, a maioria das terapias convencionais para CCR, tal como imunoterapia, são ineficazes.
– Carcinoma de Células Renais (CCR) Cromófobo
Esta forma rara de câncer renal representa aproximadamente 5% dos casos de CCR. Pensa-se que este tipo de CCR se origina a partir do mesmo tipo de célula que aquelas que formam os oncocitomas renais (vide). Tumores híbridos que contém características tanto do CCR cromófobo quanto do oncocitoma renal também foram diagnosticados. Há uma forma familiar ou herdada de CCR cromófobo (em associação com oncocitoma renal) chamada de síndrome de Birt Hogg Dubé, a qual também está associada a uma mutação em um gene específico. Raramente ocorre metástase do CCR cromófobo até tardiamente na sua evolução clínica, e uma remoção cirúrgica de doença localizada ou mesmo localmente avançada está associada, geralmente, a um excelente prognóstico. CCR cromófobo metastático é relativamente raro e nenhuma terapia padrão existe atualmente.
-Carcinoma de Células Renais Não-Classificado
Menos de 1% dos carcinomas de células renais são de tipo não-classificado e são muito raros. Eles não se encaixam em nenhum dos subtipos mais comuns de CCR. Quando examinados em microscópio, estas células de câncer não-classificadas apresentam uma estrutura e características genéticas não compatíveis com a descrição dos subtipos de CCR mais comuns. Esta categoria geralmente inclui tumores agressivos que não respondem à terapia tradicional para CCR.
-Carcinoma dos Ductos Coletores
Esta é uma variação rara e muito agressiva do câncer renal que representa menos de 1% dos casos. Esta forma de CCR é, em geral, metastática no momento do diagnóstico e é mais comum em indivíduos mais jovens. O tratamento foi direcionado no uso de regimes com base em quimioterapia, semelhante àqueles utilizados no tratamento de carcinoma de células transicionais (vide abaixo), uma vez que estes tumores não respondem às terapias tradicionais de CCR, como a bioimunoterapia.
-Carcinoma de Células Renais (CCR) medular
Esta também é uma variação muito rara e agressiva do câncer renal, apesar de ser uma variação do carcinoma dos ductos coletores. Ele está comumente associado ao traço falciforme e, portanto, é mais comum na população afro-americana. Ele representa menos de um por cento dos cânceres renais diagnosticado. A quimioterapia continua sendo o foco principal do tratamento para esta doença.
-Carcinoma de Células Renais (CCR) Sarcomatoide
Esta condição, conhecida como “diferenciação”, pode ocorrer com qualquer um dos subtipos comuns de CCR. O termo se refere ao fato de que as células do CCR – quando visualizadas em microscópio – têm aparência de células de sarcoma. A porcentagem de diferenciação de sarcomatoide é, geralmente, refletida no relato de patologia do tumor e relata a agressividade do tumor. O prognóstico associado ao CCR Sarcomatoide geralmente é desfavorável. A condição é frequentemente encontrada em pacientes cujo câncer renal realizou metástase de forma ampla. Esta forma de câncer renal é, alguma vezes, tratada com quimioterapia.
-Carcinoma de Células Transicionais do Rim (CCT)
Carcinoma de células transicionais (CCT) do rim é um tumor raro e potencialmente muito agressivo que não deve ser considerado um verdadeiro câncer renal, mas ao invés, deve ser agrupado com aqueles cânceres que se desenvolvem a partir da linha do trato urinário. Isto inclui CCT da bexiga, que é muito mais comum do que CCT do rim. Se o câncer não se espalhou, o tumor pode ser tratado por remoção cirúrgica tanto do rim quanto do ureter, embora recorrências de CCT na bexiga sejam comuns. Quando o tumor é grande ou ocorreu metástase, o prognóstico é extremamente desfavorável e as opções de tratamento são semelhantes àquelas para câncer de bexiga metastático, que inclui quimioterapia.
SUBTIPOS
Oncocitoma Renal
Este é um tumor benigno do rim que soma aproximadamente 5% de todos os tumores de rim. Não ocorre metástase destes tumores, embora possam crescer a tal tamanho no rim e invadir estruturas locais, que podem resultar em sintomas que requerem cirurgia. Eles são considerados relacionados ao CCR cromófobo e pode ser muito difícil diferenciar os dois. O tumor é tratado através de remoção parcial ou completa do rim.
A escolha do tratamento, onde o tratamento é feito, a frequência de check-ups e muitos outros aspectos do controle da doença são determinados pelo paciente e o médico. Alguns pacientes acreditam que as informações sobre o câncer renal são apresentadas em termos médicos complicados. Mas, muitas informações, incluindo os recursos recomendados neste guia são especificamente escritos para pacientes em uma linguagem fácil de entender a qual não requer treinamento especializado.
Quanto mais você souber, melhores serão suas decisões, e mais você se sentirá no controle da sua doença. O conhecimento sobre a sua doença o ajudará a se comunicar melhor com seu médico e enfermeira e aumentará sua confiança no tratamento que você recebe. Saber mais sobre o câncer renal é um passo importante para lutar efetivamente contra a doença.
Como prevenir?
NÃO FUMAR → O tabagismo aumenta significativamente o risco do câncer renal. O risco aumentado parece estar relacionado a quantidade que você fuma. O risco cai se você parar de fumar, mas leva muitos anos para se aproximar ao nível de alguém que nunca fumou;
SOBREPESO/OBESIDADE → Manter uma alimentação saúdavel. Abuse de frutas, verduras e legumes. Elas são as maiores fontes de micronutrientes e ajudam na regulação do organismo. As pessoas que estão muito acima do peso apresentam um risco mais alto de desenvolvimento de câncer de células renais. Alguns médicos acreditam que a obesidade é um fator em certa de 2 de 10 pessoas que adquirem este câncer. A obesidade pode provocar alterações em determinados hormônios que podem levar ao carcinoma de células renais;
PRATIQUE EXERCÍCIO FÍSICO → O sobrepeso e a obesidade podem provocar alterações hormonais que levam ao desenvolvimento do câncer;
MODERE NO SAL E REDUZA O AÇÚCAR → evitando a retenção de liquído, alta pressão arterial e diabetes;
BEBA ÁGUA → ela hidrata o organismo e mantém o bom funcionamento dos rins!
Fatores de Risco
Um fator de risco é qualquer coisa que afete suas chances de contrair uma doença, como um câncer. Diferentes tipos de cânceres apresentam diferentes fatores de risco. Por exemplo, a exposição sem proteção a fortes raios solares é um fator de risco para câncer de pele. Mas os fatores de risco não nos dizem tudo. Apresentar um fator de risco, ou mesmo vários fatores de risco, não significa que você terá a doença. E algumas pessoas que adquirem a doença podem não ter apresentado nenhum dos fatores de risco conhecidos. Mesmo se a pessoa com câncer renal apresentar um fator de risco, em geral é muito difícil saber o quanto aquele fator de risco pode ter contribuído para o câncer.
Fatores de risco Genéticos e Hereditários:
Algumas pessoas herdam uma tendência de desenvolver determinados tipos de câncer. O DNA que você herda dos seus pais pode conter determinadas alterações que contribuem para esta tendência de desenvolver câncer. O câncer renal pode ser causado por algumas condições raras herdadas. Pessoas com estas condições apresentam um risco muito mais alto de adquirir câncer renal, embora elas contribuam apenas para uma pequena parte dos casos no total.
Entre os fatores de risco Genéticos e Hereditários estão:
Carcinoma de Células Renais Papilar Hereditário
Pessoas com esta condição apresentam uma tendência herdada de desenvolver um ou mais carcinomas de células renais papilares, porém eles não apresentam tumores em outras partes do corpo, como é o caso de outras condições herdadas listadas aqui. Pensa-se que este distúrbio seja causado por alterações no gene MET.
Doença von Hippel-Lindau
Pessoas com esta condição frequentemente desenvolvem vários tipos de tumores e cistos (bolsas preenchidas por fluídos) em diferentes partes do corpo. Eles apresentam risco aumentado de desenvolver carcinoma de células renais de células claras, especialmente quando mais jovens. Eles também podem apresentar tumores benignos nos olhos, cérebro, medula espinhal, pâncreas e outros órgãos; e um tipo de tumor da glândula suprarrenal chamado feocromocitoma. Esta condição é provocada por mutações (alterações) no gene VHL.
Leiomiomatose Hereditária e Carcinoma de Células Renais
Pessoas com esta síndrome desenvolvem tumores de músculo liso chamados leiomiomas ou fibroides da pele e do útero (em mulheres) e apresentam um risco mais alto de desenvolver cânceres de células renais papilares. Está ligado a alterações no gene da fumarato hidratase (FH).
Síndrome Birt-Hogg-Dube
Pessoas com esta síndrome, que é caracterizada pelo desenvolvimento de pequenos tumores cutâneos benignos, apresentam um risco aumentado de desenvolver diferentes tipos de cânceres de células renais. Eles também podem apresentar tumores benignos ou malignos de vários outros tecidos. O gene ligado a esta condição é conhecido como BHD.
Oncocitoma Renal Hereditário
Algumas pessoas herdam a tendência de desenvolver um tumor de rim chamado oncocitoma, que apresenta um potencial muito baixo de ser maligno. É importante que as pessoas que apresentam causas hereditárias de câncer de células renais visitem seus médicos com frequência, particularmente se elas já têm câncer de células renais diagnosticadas. Alguns médicos recomendam testes de imagem regulares (como exames de CT) para estas pessoas.
Outros
Há alguns fatores de risco que não podem ser alterados, mas podemos aprender a observá-los e relatar qualquer alteração à equipe médica. São eles:
Histórico Familiar de Câncer Renal
As pessoas com um forte histórico familiar de câncer de células renais (sem uma das condições herdadas conhecida listada acima) também apresentam alta chance de desenvolvimento deste câncer. Este risco é ainda mais alto em irmãos (irmãos ou irmãs) daqueles afetados. Se não está claro se é devido à genética, uma exposição ambiental compartilhada, ou alguma combinação destes.
Alta Pressão Arterial
O risco de câncer renal é mais alto em pessoas com alta pressão arterial. Alguns estudos sugeriram que determinados medicamentos utilizados para tratar alta pressão arterial pode desenvolver o risco de câncer renal, mas é difícil dizer se a condição ou a medicação (ou ambos) podem ser a causa do risco aumentado.
Determinados Medicamentos
Fenacetina, um remédio popular para alívio de dor com venda livre, esteve ligado ao câncer de células renais no passado. Alguns estudos sugeriram que diuréticos (medicamentos que tratam a alta pressão arterial provocando que os rins removam o sal e fluído do corpo) podem estar ligados ao carcinoma de células renais. Não está claro se a causa é dos medicamentos ou da alta pressão arterial em si. Se você precisa de diuréticos, você deve tomá-los. Se não precisa, evite-os para tentar reduzir o risco de câncer renal.
Doença de Rim Avançada
Pessoas com doença de rim avançada, especialmente aqueles que precisam de diálise, apresentam um risco mais alto de carcinoma de células renais. A diálise é um tratamento utilizado para remover toxinas do seu corpo caso os rins não funcionem apropriadamente.
Gênero
O carcinoma de células renais e quase duas vezes tão comum em homens quanto em mulheres. Os homens estão provavelmente mais propensos a fumar e a estarem expostos a elementos químicos que provocam câncer no trabalho, que podem contribuir com uma parte da diferença.
Raça
Negros apresentam uma taxa ligeiramente mais alta de câncer de células renais do que brancos. As razões para isto não estão claras.
Sabemos o que causa o câncer renal?
Embora muitos fatores de risco possam elevar sua chance de desenvolver câncer renal, não se sabe ainda de forma exata como alguns desses fatores de risco tornam as células do rim cancerígenas.
Alterações Genéticas
Pesquisadores estão começando a entender como algumas alterações no DNA podem resultar na modificação de células do rim normais em células cancerígenas.
DNA é a molécula química em cada uma de nossas células que compõe nossos genes – as instruções sobre como nossas células funcionam.
Nós geralmente parecemos com os nossos pais porque eles são a fonte de nosso DNA . Contudo, o DNA afeta mais do que nossa aparência.
Alguns genes contêm instruções para controle de quando nossas células devem crescer, se dividir e morrer. Determinados genes que aceleram a divisão celular são chamados oncogenes. Outros genes que diminuem a velocidade da divisão celular ou fazem com que as células morram no momento certo são denominados genes supressores de tumor.
O câncer pode ser causado por mutações do DNA (alterações) que ativam os oncogenes ou desativam os genes supressores de tumor.
Mutações Genéticas Herdadas
Determinadas alterações do DNA herdadas podem levar a condições correntes em algumas famílias que aumentam o risco de câncer renal.
Estas síndromes, que provocam uma pequena parte de todos os cânceres renais, foram descritas na seção Fatores de Risco.
Por exemplo, o gene VHL é um gene supressor de tumor. Ele normalmente ajuda a impedir que as células cresçam fora de controle. As mutações (alterações) neste gene podem ser herdada de um dos pais, provocando a doença von Hippel-Lindau. Quando ocorre mutação no gene VHL, ele não mais suprime o crescimento anormal e é mais provável que o câncer renal se desenvolva.
Os genes ligados à leiomiomatose hereditária, ao carcinoma de células renais (o gene da fumarato hidratase) e à síndrome Birt-Hogg-Dube (o gene BHD) também são genes supressores de tumor, e as alterações herdadas nestes genes também levam a um risco aumentado de câncer renal.
Pessoas com carcinoma de células renais papilar hereditário herdam alterações no oncogene MET que podem provocar que fique “ativo” o tempo todo. Isto torna a pessoa mais propensa a desenvolver câncer de células renais papilar.
Mutações Genéticas Adquiridas
A maioria das mutações de DNA relacionadas ao câncer de mama, entretanto, ocorre durante a vida da pessoa ao invés de ser herdada. Estas mutações adquiridas de oncogenes e/ou dos genes supressores de tumor podem resultar de fatores como exposição a elementos químicos que provocam câncer (como aqueles encontrados no tabaco), porém em muitos casos a causa destas alterações não é conhecida.
Cerca de 3 de 4 pessoas com câncer de células renais claras esporádico (não-herdado) apresentam alterações no gene VHL que provoca que este não funcione apropriadamente. Estas alterações foram adquiridas durante a vida ao invés de serem herdadas.
Outras alterações genéticas também podem provocar carcinomas de células renais. Os pesquisadores continuam a procurar estas alterações.
Algum progresso foi alcançado na compreensão em como o tabaco aumenta o risco de desenvolvimento de carcinoma de células renais. Muitos dos elementos que provocam câncer no tabaco são absorvidos pela corrente sanguínea pelos pulmões. Como os rins filtram este sangue, muitos destes elementos tornam-se altamente concentrados nos rins.
Vários destes elementos químicos são conhecidos por danificar o DNA das células renais de forma que pode tornar células normais em cancerígenas.
A obesidade, outra causa deste câncer, altera o equilíbrio de alguns dos hormônios do corpo. Os pesquisadores estão agora aprendendo como determinados hormônios ajudam a controlar o crescimento (tanto normal quanto anormal) de muitos tecidos diferentes no corpo, incluindo os rins.
Conhecimento das alterações genéticas que podem levar ao câncer de mama está sendo utilizado para ajudar a desenvolver novos tratamentos para esta doença. Por exemplo, os pesquisadores agora sabem que o gene VHL normalmente impede que as células produzam uma substância chamada fator do crescimento endotelial vascular (VEGF). Esta substância provoca a formação de novos vasos sanguíneos, dos quais os tumores precisam para sobreviver e crescer. Medicamentos recentes que têm como alvo o VEGF estão agora sendo utilizados para tratar o câncer renal.
Alguns possíveis sinais e sintomas de câncer renal incluem:
> sangue na urina (hematúria);
> dor lombar em um lado (não provocada por lesão);
> uma massa ou inchaço no lado ou na região lombar;
> fadiga;
> perda de peso não explicada;
> febre que não é causada por um resfriado ou outra infecção e que não passa após poucas semanas;
> inchaço dos tornozelos e pernas (edema);
Estes sintomas podem ser causados pelo câncer, mas com mais frequência se dão devido a doenças não-cancerosas. Por exemplo, sangue na urina pode ser um sinal de câncer renal, bexiga ou de próstata, mas com muita frequência é provocado por infecção na bexiga ou pedra no rim. Ainda, se você apresentar algum destes sintomas, consulte um médico, assim a causa pode ser avaliada e tratada, se necessário.
Como o Câncer Renal é Diagnosticado?
Muitos cânceres renais são encontrados regularmente de forma precoce, enquanto eles ainda estão confinados no rim. Porém, outros são encontrados em um estágio mais avançado. Há algumas razões para isto:
> Estes cânceres podem, algumas vezes, se tornar muito grandes sem provocar nenhuma dor ou outros problemas;
> Devido ao fato do rim estar muito adentro do corpo, pequenos tumores do rim não podem ser observados ou sentidos durante um exame físico;
> Não há testes simples que possam ser utilizados para examinar o câncer renal em pessoas que não estão em risco aumentado.
Um teste de urina de rotina, que, às vezes, é parte de um exame médico completo, pode encontrar pequenas quantidades de sangue na urina de algumas pessoas com câncer de células renais precoce. Porém, há muitas outras causas de sangue na urina, incluindo infecções do trato urinário, infecções da bexiga, câncer da bexiga e condições benignas do rim (não cancerosas), tais como pedras no rim.
Por outro lado, algumas pessoas com câncer renal não apresentam sangue na urina até que o câncer esteja muito grande e possa ter se espalhado para outras partes do corpo. Exames de imagem, tais como exames de tomografia computadorizada (CT) e exames de imagem por ressonância magnética (MRI) podem encontrar pequenos carcinomas de células renais. Mas estes exames são caros e nem sempre revelam tumores benignos de pequenos carcinomas de células renais. Por estas razões, os médicos geralmente recomendam CT e MRI para detecção precoce de câncer renal apenas em pessoas que apresentam determinados fatores de risco, tais como doença von Hippel-Lindau (VHL) ou outras condições herdadas. Alguns médicos também recomendam que pessoas com doenças de rim tratadas por diálise em longo prazo realizem testes periódicos (exames de CT ou MRI) para procurar por câncer renal. Em geral, cânceres renais são encontrados incidentalmente durante exames para algumas outras doenças, tais como doença de vesícula biliar. Estes cânceres geralmente não provocam dor ou desconforto no momento da descoberta. A taxa de sobrevida para câncer renal descoberto desta forma é muito alta, pois estes cânceres geralmente são descobertos em um estágio muito precoce.
Saiba mais sobre diagnóstico precoce:
É importante dizer ao seu médico se familiares (parentes de sangue) apresentam ou apresentaram câncer renal, especialmente quando jovens, ou se eles foram diagnosticados com uma condição herdada ligada a este câncer, como doença VHL. Seu médico pode recomendar que você considere o teste genético. O teste genético para estas condições é utilizado apenas em pessoas com sinais clínicos destas condições e em seus parentes de sangue. Antes de realizar os testes genéticos, é importante falar com um consultor genético, assim você entende o que os testes podem – e não podem – dizer a você, e o que alguns resultados significariam. Os testes genéticos procuram mutações genéticas que provocam estas condições no seu DNA. Eles são utilizados para diagnosticar estas condições herdadas, não o câncer renal em si. Seu risco pode estar aumentado se você apresentar uma destas condições, mas isto não significa que você apresenta (ou definitivamente apresentará) câncer renal. Se você foi diagnosticado com uma destas condições, você pode precisar de frequentes exames de CT ou MRI para procurar por câncer renal.
Para o dignóstico do câncer renal são utilizados exames de imagem e laboratóriais. Abaixo listados os exames necessários para diagnosticar o câncer renal:
Exames de Imagem
Exames por imagem utilizam raios-X, campos magnéticos ou substâncias radioativas para criar fotos de dentro do seu corpo. Exames de imagem podem ser realizados por um número de motivos, incluindo ajudar a descobrir se a área suspeita pode ser cancerosa, saber o quão longe o câncer pode ter se espalhado e ajudar a determinar se o tratamento foi eficaz. Diferente da maioria dos outros cânceres, os médicos podem com frequência ter certeza sobre o diagnóstico do câncer renal sem precisar realizar uma biópsia (remoção de uma amostra do tumor para ser observado em microscópio). Em muitos casos, os exames de imagem podem dar aos médicos uma quantidade razoável de certeza que uma massa do rim é (ou não) cancerosa. Em alguns casos, no entanto, uma biópsia pode ser necessária para ter certeza. Exames de tomografia computadorizada (CT), exames de imagem por ressonância magnética (MRI), pielogramas intravenosos e ultrassom podem ser muito úteis no diagnóstico na maioria dos tipos de tumores renais, embora os pacientes raramente precisem de todos estes exames. Outros exames descritos aqui, como raios-X do tórax e exames ósseos são utilizados com mais frequência para ajudar a determinar se o câncer se propagou (ocorreu metástase) para outras partes do corpo.
Exame de Tomografia Computadorizada (CT ou CAT)
O exame de Exame de Tomografia Computadorizada (CT ou CAT) consiste em um exame de raio-X que produz imagens seccionais cruzadas detalhadas do seu corpo. Ao invés de tirar uma fotografia, como um raio-X convencional, o aparelho de CT obtém diversas imagens conforme gira ao seu redor, enquanto você está deitado em uma mesa. Então, um computador combina essas imagens na forma de imagens de fatias da parte do corpo que está sendo estudada. Diferente de um raio-X convencional, um exame de CT cria imagens detalhadas dos tecidos moles no corpo. Depois de obtido o primeiro grupo de imagens, pode ser solicitado que você beba uma solução de contraste e/ou você pode receber um cateter IV (intravenoso) por meio do qual é injetado um corante de contraste. Ele ajuda a delinear melhor as estruturas do seu corpo. Em seguida, se obtém um segundo grupo de imagens.
O contraste pode provocar um pouco de rubor (uma sensação de calor, especialmente na face). Algumas pessoas são alérgicas e apresentam urticária. Raramente, podem ocorrer reações mais sérias como dificuldades para respirar ou queda da pressão arterial. Não deixe de informar o médico caso você sofra ou já tenha sofrido alguma reação a qualquer material de contraste utilizado para raios-X.
Exames de CT são mais demorados do que raios-X convencionais. Você precisa ficar deitado em uma mesa durante sua realização. Durante o exame, a mesa se movimenta para dentro e para fora do aparelho, uma máquina em formato de anel que envolve completamente a mesa. Você pode se sentir um pouco confinado pelo anel em que deve se deitar enquanto as imagens são obtidas.
Nos últimos anos, a CT espiral (também conhecida como CT helicoidal) se tornou disponível em muitos centros médicos. Este tipo de exame de CT utiliza uma máquina mais rápida. A parte da máquina que obtém a imagem roda em volta do corpo continuadamente, permitindo que os médicos coletem as imagens mais rapidamente do que com a CT padrão. Isto reduz a chance de imagens “borradas” decorrentes do movimento de respiração. Também diminui a dose de radiação recebida durante o exame. A maior vantagem pode ser que as “fatias” de imagem que ele obtém são mais finas, o que proporciona imagens mais detalhadas e permite que médicos olhem as áreas suspeitas de diferentes ângulos.
O exame de CT é um dos exames mais úteis para achar e olhar uma massa dentro do rim. Ele também é útil para verificar se um câncer se espalhou, ou não, para órgãos e tecidos além do rim. O exame de CT fornecerá informações precisas sobre o tamanho, formato e posição de um tumor, e pode ajudar a encontrar linfonodos maiores que possam conter câncer.
Imagem por Ressonância Magnética (MRI)
Assim como os exames de Tomografia Computadorizada (CT), os exames de Imagem por Ressonância Magnética (MRI) fornecem imagens detalhadas de tecidos moles no corpo.
Exames de MRI são utilizados com menos frequência do que os exames de CT em pessoas com câncer renal. Eles podem ser realizados em casos onde os exames de CT não são práticos, tais como se a pessoa for alérgica ao contraste de CT.
Exames de MRI também podem ser realizados se houver uma chance do câncer envolver uma veia principal no abdômen (veia cava inferior). Finalmente, eles podem ser utilizados para procurar possível propagação do câncer para o cérebro ou para a medula espinhal se uma pessoa apresentar sintomas que sugerem que este possa ser o caso.
Ultrassom (ultrassonografia ou US)
O ultrassom utiliza ondas sonoras para criar imagens de órgãos internos.
Para este exame, um pequeno instrumento semelhante a um microfone chamado transdutor é colocado na pele próximo ao rim. Ele emite ondas sonoras e capta os ecos conforme eles são refletidos pelos tecidos no rim. Os ecos são convertidos por um computador em uma imagem em preto e branco que é exibida em uma tela de computador. Este exame é indolor e não expõe você à radiação.
O ultrassom pode ser útil para determinar se uma massa do rim é sólida ou preenchida por fluído. Os modelos de eco produzidos pela maioria dos tumores do rim parecem diferentes daqueles do tecido do rim normal.
Diferentes modelos de eco também podem distinguir alguns tipos de tumores benignos e malignos do rim um do outro. Se uma biópsia de rim for necessária, este exame pode ser utilizado para guiar uma agulha da biópsia na massa para obter uma amostra.
Exame de Tomografia por Emissão de Pósitron (PET SCAN)
Exames de PET SCAN envolvem a injeção de uma forma de açúcar radioativo (conhecido como fluorodeoxiglicose ou FDG) no sangue. A quantidade de radioatividade utilizada é muito baixa.
Como as células cancerosas do corpo crescem rapidamente, elas absorvem grandes quantidades do açúcar radioativo. Uma câmera especial pode, assim, gerar uma imagem de áreas de radioatividade do corpo. A imagem não é extremamente detalhada como um exame de CT ou MRI, mas proporciona informações úteis sobre o corpo todo.
Este exame pode ser útil para observar se o câncer pode ter se espalhado para os linfonodos próximos ao rim. Exames de PET também podem ser úteis quando o médico acredita que o câncer possa ter se espalhado, mas não tem conhecimento de onde isso ocorreu. Exames de PET podem ser utilizados ao invés de diversos raios-X diferentes, pois eles realizam varredura do corpo inteiro.
Algumas máquinas mais recentes conseguem realizar tanto um exame de PET quanto um exame de CT ao mesmo tempo (exame PET/CT). Isso permite ao radiologista comparar áreas de maior radioatividade no PET com a aparência da mesma área na CT.
Pielograma Intravenoso (IVP)
Um pielograma intravenoso é um raio-X do sistema urinário realizado após um corante especial ter sido injetado na veia. Este corante sai da corrente sanguínea para os rins e, então, passa pelos ureteres e bexiga.
Um IVP pode ser útil para encontrar anormalidades do trato urinário, tais como câncer, mas você pode não precisar de um IVP caso já tenha realizado uma CT ou MRI.
Angiografia
Assim como IVP, este exame de raio-X também utiliza um corante de contraste. Um cateter é geralmente preso a uma artéria de grande porte na sua perna na artéria que segue para o rim (artéria renal). O corante é, então, injetado na artéria para contornar os vasos sanguíneos.
Como a angiografia pode contornar os vasos sanguíneos que alimentam o tumor do rim, ela pode ajudar o cirurgião a planejar uma cirurgia. A angiografia também pode ajudar a diagnosticar cânceres renais uma vez que os vasos sanguíneos geralmente apresentam uma aparência especial com este exame.
Raio-X do Tórax
Se o câncer renal foi diagnosticado (ou há suspeita), um raio-X plano do seu tórax pode ser realizado para observar se o câncer se propagou para os pulmões. Isto é muito improvável, a menos que o câncer esteja muito avançado. Este raio-X pode ser realizado em qualquer contexto ambulatorial. Se os resultados forem normais, provavelmente você não apresenta câncer nos pulmões.
Exame Ósseo
Um exame ósseo pode ajudar a mostrar se o câncer sofreu metástase (se espalhou) para os ossos. Nesse exame, é injetada uma pequena quantidade de material de baixo nível de radioatividade em uma veia (por via intravenosa, ou IV). A substância se deposita nas áreas do osso comprometido por todo o esqueleto, no decorrer de algumas horas. Então, você fica deitado sobre uma mesa por cerca de 30 minutos enquanto uma câmera especial detecta a radioatividade e gera uma imagem do seu esqueleto.
Áreas de alterações ósseas ativas como “hot spots” no seu esqueleto – ou seja, elas atraem a radioatividade. Essas áreas podem sugerir a presença de câncer metastático, no entanto, a artrite e outras doenças ósseas também podem produzir o mesmo padrão. Para distinguir entre essas condições, sua equipe de cuidados oncológicos pode utilizar outros exames de imagem, como raios-x simples ou exames de CT e MRI, para conseguir uma visualização melhor das áreas realçadas, ou podem até mesmo colher amostras do osso para biópsia.
Exames ósseos são realizados principalmente quando há motivo para pensar que o câncer possa ter se espalhado para os ossos (pois uma pessoa apresenta sintomas como dor óssea). Exames de PET geralmente também podem mostrar a propagação do câncer para os ossos, portanto, se você realizou um exame de PET você pode não precisar de um exame ósseo.
Exames Laboratoriais
Exames laboratoriais geralmente não são utilizados para diagnosticar câncer renal, mas eles podem, algumas vezes, dar a primeira pista de que pode haver um problema com os rins. Eles também são realizados para ter uma ideia da saúde geral da pessoa e para ajudar a dizer se o câncer pode ter se espalhado para outras áreas. Antes da cirurgia, eles podem ajudar a dizer se uma pessoa é saudável o suficiente para realizar a operação.
Exame de Urina (Urinálise)
O Exame de Urina (Urinálise) é, algumas vezes, parte de um exame físico completo, mas ele pode não ser realizado como parte de exames físicos de rotina. É provável que seja um dos primeiros exames realizados caso o câncer renal seja uma possibilidade.
Exames microscópicos e químicos são realizados na urina para procurar pequenas quantidades de sangue e outras substâncias não observadas a olho nu. Cerca de metade dos pacientes com câncer de células renais apresentam sangue na urina. Algumas vezes, exame microscópico especial de amostras da urina (chamado citologia da urina) mostrará células cancerosas reais na urina.
Hemograma
O hemograma pode detectar achados algumas vezes observados com câncer de células renais. Anemia (pouquíssimos eritrócitos) é muito comum. Com menos frequência, uma pessoa pode apresentar muitos eritrócitos, pois o câncer renal produz um hormônio (eritropoietina) que provoca que a medula óssea produza mais eritrócitos. As contagens de sangue também são importantes para se certificar que uma pessoa é saudável o suficiente para uma cirurgia.
Exames de Bioquímica do Sangue
Exames de bioquímica do sangue geralmente são realizados em pessoas que possam apresentar câncer renal, uma vez que ele pode afetar os níveis de determinados elementos químicos no sangue. Por exemplo, altos níveis de enzimas hepáticas são encontrados algumas vezes, embora os motivos para isso não sejam conhecidos. Altos níveis de cálcio no sangue podem indicar que o câncer se espalhou para os ossos e pode, portanto, alertar o médico para solicitar um exame ósseo.
Biópsia por Aspiração com Agulha Fina
Este exame é raramente utilizado para diagnosticar tumores de rim. Estudos por imagem geralmente fornecem informações suficientes para um cirurgião decidir se a operação é ou não necessária. Algumas vezes a biópsia por aspiração com agulha fina (FNA) é utilizada para obter pequena amostra das células de uma área suspeita se os resultados do exame de imagem não forem conclusivos o suficiente para garantir a remoção do rim. Ela também pode ser realizada para confirmar o diagnóstico de câncer se a saúde da pessoal for muito deficiente para cirurgia e outros tratamentos locais (tais como embolização arterial ou crioterapia) estão sendo considerados. Para este exame, a pele onde a agulha será inserida é, em primeiro lugar, adormecida com anestesia local. O médico direciona uma agulha vazia na área enquanto observa seu rim com exames de ultrassom ou CT. Diferente do ultrassom, a CT não fornece uma imagem contínua, então a agulha é inserida na direção da massa, uma imagem de CT é obtida e a direção da agulha é orientada com base na imagem. Isto é repetido algumas vezes até a agulha estar dentro da massa. Uma pequena amostra da área-alvo é sugada (aspirada) para uma seringa e observada em microscópio para observar se células cancerosas estão presentes. Em casos onde os médicos pensam que o câncer renal possa ter se espalhado para outros locais, eles podem realizar uma biópsia do local metastático ao invés do rim.
Grau de Fuhrman
O grau de Fuhrman é determinado pela observação das células do câncer renal (obtidas durante uma biópsia ou durante cirurgia) em um microscópio. Ele é utilizado por muitos médicos como uma maneira de descrever o quão agressivo o câncer provavelmente pode ser. O grau é baseado em o quanto os núcleos das células cancerosas (parte de uma célula na qual o DNA é armazenado) se parece com aqueles de células de um rim normal. Os cânceres de células renais geralmente são graduados em uma escala de 1 até 4. Os cânceres de células renais grau 1 têm núcleos celulares que diferem muito pouco dos núcleos celulares de um rim normal. Estes cânceres normalmente crescem e se espalham lentamente e tendem a apresentar uma boa perspectiva. No outro extremo, núcleos de câncer de células renais grau 4 são muito diferentes de núcleos de células de um rim normal e apresentam um pior prognóstico. Embora o tipo celular e o grau algumas vezes sejam úteis na previsão do prognóstico, o estágio do câncer está longe de ser a melhor previsão de sobrevida. O estágio descreve o tamanho do câncer e o quanto ele se espalhou além do rim.
Como é tratado?
O tratamento varia de pessoa para pessoa. A escolha depende muito do estágio do câncer, do estilo de vida do paciente e da alimentação. Após a determinação do câncer e de seu estágio, a equipe de cuidados oncológicos discutirá com o paciente as opções de tratamento. No caso do câncer renal, as opções de tratamento podem incluir cirurgia, terapia por radiação, terapia-alvo, imunoterapia, quimioterapia ou outras dessas combinações, dependendo dos fatores acima mencionados.
Tipos de Tratamento
Cirurgia
A cirurgia é o principal tratamento para a maioria dos carcinomas de células renais. As chances de sobreviver a um câncer de célula renal sem cirurgia são pequenas. Dependendo do estágio e do local do câncer e outros fatores, a cirurgia pode ser usada para remover tanto o câncer com alguns tecidos circundantes do rim quanto o rim em sua totalidade.
Radioterapia
A Radioterapia usa radiação de alta energia para matar as células cancerígenas. A terapia por feixe externo foca a radiação a partir do lado de fora do corpo sob o câncer. É como fazer um raio-x, mas a radiação é muito mais intensa. O procedimento em si é indolor. A radioterapia pode ser usada para tratar o câncer renal se a saúde geral da pessoa estiver muito debilitada para passar por cirurgia. Infelizmente, os cânceres renais não são muito sensíveis à radiação. Usar radioterapia antes ou após a remoção do câncer, não é rotineiramente recomendado porque os estudos não mostraram que ela melhora as taxa de sobrevida.
Quimioterapia
Quimioterapia usa medicamentos anticâncer que são administrados na veia ou pela boca (em forma de pílulas). Esses medicamentos entram na corrente sanguínea e alcançam todas as áreas do corpo, o que torna o tratamento potencialmente útil para o câncer que se disseminou (metastatizado) para os órgãos além dos rins.Infelizmente, as células do câncer renal são geralmente resistentes à quimioterapia, e não existe nenhuma maneira padrão de tratá-las com esses medicamentos. A quimioterapia é geralmente reservada para cânceres onde os medicamentos alvo e/ou imunoterapia não são eficazes.
Terapia-alvo
A terapia alvo é considerada uma medida terapêutica que veio revolucionar o tratamento do câncer, causando menos danos às células sadias. Utilizam anticorpos monoclonais, capazes de limitar o crescimento do tumor, em uma ação semelhante ao nosso sistema imunológico. Cerca de 20 a 25% dos casos se beneficiam dessa alternativa.
Imunoterapia
Segundo o Instituto Nacional do Câncer – INCA, é chamado de imunoterapia o tratamento do câncer que promove a estimulação do sistema imunológico, por meio do uso de substâncias modificadoras da resposta biológica. A imunoterapia é classificada em ativa e passiva, de acordo com as substâncias utilizadas e os seus mecanismos de ação. Na imunoterapia ativa, substâncias estimulantes e restauradoras da função imunológica (imunoterapia inespecífica) e as vacinas de células tumorais (imunoterapia específica) são administradas com a finalidade de intensificar a resistência ao crescimento tumoral. Na imunoterapia passiva ou adotiva, anticorpos antitumorais ou células mononucleares exógenas são administradas, objetivando proporcionar capacidade imunológica de combate a doença.
Curiosidades sobre o câncer renal:
- Você sabe a quantidade ideal que você deve consumir de água por dia? Saiba que cada pessoa possui uma quantidade ideal. Descubra qual a sua no site do Instituto Espaço de Vida e comece agora a beber a sua quantidade ideal!
- Voce sabe quanto pesa o seu rim? 150 gramas é o peso de cada um dos seus rins.
- Os cálculos Renais aumentam cerca de 30% durante o verão. Por isso, fique atento!
Como o Câncer Renal é Classificado?
O estadiamento é o processo de descobrir o quanto o câncer se espalhou. Seu tratamento e prognóstico (a previsão de chances de sobrevida) dependem, em grande parte, do estágio do câncer.
O estadiamento está baseado em resultados de exame físico, biópsias e exames de imagem (exame de CT, raio-X do tórax, exame de PET, etc.).
Na verdade, há 2 tipos de estadiamento para o câncer renal. O estágio clínico é a melhor estimativa do seu médico da extensão da sua doença, com base nos resultados de exame físico, exames laboratoriais e qualquer estudo de imagem que você tenha realizado. Se você realizar cirurgia, seus médicos também podem determinar o estágio patológico, que é baseado em alguns fatores como estágio clínico, mais o que for encontrado durante a cirurgia e exame do tecido removido. Isto significa que se você realizar uma cirurgia, o estágio do câncer pode realmente mudar depois disso (se foi descoberto que o câncer se espalhou mais do que estava suspeito, por exemplo). Provavelmente, o estadiamento patológico é mais preciso que o clínico, já que permite ao médico obter uma impressão direta da extensão do câncer.
Sistema de Estadiamento AJCC (TNM)
O sistema de estadiamento é uma maneira padronizada no qual a equipe de tratamento oncológico descreve a extensão do câncer. O sistema de estadiamento mais comumente utilizado é o da American Joint Committee on Cancer (Comitê da Junta Americana do Câncer) (AJCC), algumas vezes também conhecido como sistema TNM. O sistema TNM descreve 3 informações-chave:
> T indica o tamanho do tumor principal (primário) e se ele cresceu para as áreas próximas.
> N descreve a extensão de propagação para os linfonodos próximos (regionais). Os linfonodos são pequenos grupos de células do sistema imune em formato de feijão que são importantes na luta contra infecções.
> M indica se o câncer se espalhou (sofreu metástase) para outros órgãos do corpo. (Os locais mais comuns de propagação são para os pulmões, ossos, fígado e linfonodos distantes).
Números ou letras aparecem após T, N e M para fornecer mais detalhes sobre cada um destes fatores. Os números 0 a 4 indicam gravidade crescente. A letra X significa “não pôde ser avaliado, pois as informações não estavam disponíveis”.
Categorias T para Câncer Renal
TX: O tumor primário não pode ser avaliado (informações não disponíveis).
T0: Nenhuma evidência de tumor primário.
T1a: O tumor mede 4 cm (cerca de 11/2 polegadas) em sua extremidade ou é menor e está limitado ao rim.
T1b: O tumor mede mais que 4 cm, mas não maior que 7 cm (cerca de 2 ¾ polegadas) em sua extremidade e ainda está limitado ao rim.
T2: O tumor mede mais que 7 cm em sua extremidade mas ainda é limitado ao rim.
T3a: O tumor se espalhou pela glândula suprarrenal (que está situada sobre o rim) ou dentro do tecido adiposo ao redor do rim, mas não para além da camada fibrosa que circunda o rim e as proximidades do tecido adiposo (Fáscia de Gerota).
T3b: O tumor se espalhou para dentro da veia principal que leva para fora do rim (veia renal) e/ou a parte da maior veia que leva para o coração (veia cava) que está dentro do abdome.
T3c: O tumor atingiu a parte da veia cava que está dentro do tórax ou invadiu a parede da veia cava.
T4: O tumor se espalhou para além da fáscia de Gerota (camada fibrosa ao redor do rim e próximo do tecido adiposo).
Categorias N para Câncer Renal
NX: Os linfonodos regionais (proximidades) não podem ser avaliados (informação não disponível).
N0: Não se espalhou nos arredores dos linfonodos.
N1: Espalhou-se para os arredores de 1 linfonodo.
N2: Espalhou-se para os arredores de mais de 1 linfonodo.
Categorias M para Câncer Renal
MX: A presença de metástase distante não pode ser avaliada (informação não disponível).
M0: Não se espalhou para os linfonodos distantes ou outros órgãos.
M1: Presença de metástase distante; inclui a propagação para os linfonodos distantes e/ou para outros órgãos (tais como pulmões, ossos ou cérebro).
Grupamento por Estágio
Uma vez que as categorias T, N e M foram determinadas, esta informação é combinada para determinar o estágio global de I, II, III ou IV. O estágio identifica cânceres que apresentam um prognóstico semelhante, e portanto, são tratados de maneira semelhante. Os pacientes com estágio de menor número tendem a apresentar prognósticos melhores.
Estágio I
T1a-T1b, N0, M0: O Tumor mede 7 cm ou menos e é limitado ao rim. Não há disseminação para os linfonodos ou órgãos distantes.
Estágio II
T2, N0, M0: O tumor mede mais que 7 cm, mas ainda é limitado ao rim. Não há disseminação para os linfonodos ou órgãos distantes.
Estágio III
Diferentes combinações de categorias T e N são incluídas neste estágio.
T3a-T3c, N0, M0: O tumor principal atingiu a glândula suprarrenal, o tecido adiposo ao redor do rim, a veia renal e/ou a veia principal (veia cava) levando do rim ao coração. Ele não se espalhou para além da fáscia de Gerota. Não há disseminação para os linfonodos ou órgãos distantes.
T1a-T3c, N1, M0: O tumor principal pode ser de qualquer tamanho e pode estar fora do rim, mas não se espalhou para além da fáscia de Gerota. O câncer se espalhou para os arredores de 1 linfonodo mas não se espalhou para os linfonodos distantes ou outros órgãos.
Estágio IV
Existem diversas combinações de categorias T, N e M que estão incluídas neste estágio.
T4, N0-N1, M0: O tumor principal invadiu além da fáscia de Gerota. Espalhou-se para os arredores de mais de 1 linfonodo. Não se espalhou para os linfonodos distantes ou outros órgãos.
Qualquer T, N2, M0: O tumor principal pode ter qualquer tamanho e pode estar fora do rim. O câncer se espalhou para os arredores de mais de 1 linfonodo mas não se espalhou para os linfonodos distantes ou outros órgãos.
Qualquer T, Qualquer N, M1: O tumor principal pode ter qualquer tamanho e pode estar fora do rim. Pode ter se espalhado ou não para perto dos linfonodos. Espalhou-se para os linfonodos distantes e/ou outros órgãos.
Outros Sistemas
Embora o sistema de classificação TNM seja útil, alguns médicos têm apontado que existem outros fatores além da extensão do câncer que devem ser considerados na determinação do prognóstico e tratamento.
Universidade da Califórnia em Los Angeles (UCLA) Sistema de Classificação Integrado
Este é um sistema mais complexo porém provavelmente mais preciso. Junto com o estágio do câncer, leva em consideração a saúde global da pessoa e o grau de Fuhrman do tumor para dividir pessoas em grupos de risco baixo, intermediário e alto. Você pode querer perguntar ao seu médico se ele ou ela usa este sistema e como ele pode se aplicar ao seu caso.
Atualmente, o câncer renal, representa cerca de 3% das doenças malignas em adultos no mundo. No Brasil, surgiu mais de 580 mil casos novos até o final de 2015, sendo duas vezes mais frequente nos homens que nas mulheres. O tipo mais comum do câncer renal é o carcinoma de células renais, que representa 90% dos casos, e se origina nos rins, podendo se espalhar pelo corpo. Dados publicados pelo Globocan, um projeto da Organização Mundial da Saúde que visa coletar, organizar e divulgar dados estimativos da incidência e mortalidade dos tipos mais comuns de câncer no mundo, apontam que, em 2015, 6.768 pessoas receberam o diagnóstico de câncer de rim no Brasil, sendo 4.068 homens e 2.700 mulheres. A maioria das pessoas com câncer renal são mais velhas. A idade média das pessoas quando diagnosticadas é de 65 anos. O câncer de rim é muito raro em pessoas com menos de 45 anos de idade. Ele está entre os 10 tipos de cânceres mais comuns em homens e mulheres. No geral, o risco de desenvolver câncer de rim é cerca de 1 em 63 (1,6%).
Sobre os Rins:
Os rins são um par de órgãos em formato de um feijão. Um rim está localizado do lado esquerdo e o outro do lado direito da coluna vertebral. Ambos estão protegidos pela caixa torácica. A principal função dos rins é filtrar o sangue e remover do corpo o excesso de água, sal e produtos residuais. Os produtos residuais filtrados são concentrados na urina. Os rins também ajudam a verificar se o corpo tem eritrócitos (também conhecidos como glóbulos vermelhos ou hemácias) suficientes. Os rins também atuam secretando substâncias importantes para nossa saúde. Entre suas funções, pode-se destacar a manutenção do equilíbrio de eletrólitos no corpo, como sódio, potássio, cálcio, magnésio, fósforo, bicarbonato etc.; a regulação do equilíbrio ácido-básico, mantendo o pH sanguíneo constante; a excreção de substâncias exógenas, como medicações; e a produção de hormônios, como aldosterona e prostaglandinas.
O câncer de rim é também conhecido como hipernefroma ou adenocarcinoma renal. Existem vários tipos de câncer renal. O mais frequente é o câncer renal de células claras, sendo responsável por 85% dos tumores diagnosticados. Entenda sobre o Câncer Renal de Células Claras: O CCR de célula clara é o tipo de célula associado com a mutação no gene von Hippel Lindau (VHL) no câncer renal hereditário. De fato, aproximadamente 70% dos casos não hereditários de CCR de células claras também apresentam mutação no aVHL.
Conheça os Tipos de Câncer Renal:
– Carcinoma de Células Renais (CCR)
Nem todos os cânceres renais são os mesmos. Há um crescente entendimento entre os médicos e pesquisadores de que há diferentes subtipos de CCR e que eles se comportam de formas completamente diferentes, tanto com relação ao quanto são agressivos no paciente quanto como eles respondem ao tratamento. Há dez ou quinze anos, era comum para um relato de patologia de um paciente com câncer renal se ler simplesmente Carcinoma de Células Renais. Hoje, este diagnóstico simples é considerado incompleto. A identificação do subtipo específico ou tipo de célula (histologia) do câncer renal pode ser tão importante na determinação do prognóstico do paciente quanto saber o estágio e o grau do CCR. Seu médico deve lhe oferecer informações sobre a histologia, grau e estágio do seu câncer renal. Em caso negativo, você deve se sentir confortável em pedir estas informações uma vez que é uma parte importante do seu planejamento de tratamento.
Os subtipos de CCR vêm da descrição da aparência das células e outras características. Eles incluem:
– Carcinoma de Células Renais (CCR) de Células Claras
Esta é a forma mais comum de câncer renal e representa entre 66% e 75% de todos os casos. O CCR de célula clara é o tipo de célula associado com a mutação no gene von Hippel Lindau (VHL) no câncer renal hereditário. De fato, aproximadamente 70% dos casos não hereditários de CCR de células claras também apresentam mutação no aVHL. Muito da pesquisa atual, que tenta identificar novos tratamentos efetivos para pacientes com doença localmente avançada ou metastática, foca neste subtipo da doença, uma vez que é o tipo mais comum de CCR.
Quando o tumor não está espalhado, o prognóstico é muito bom depois de excisão cirúrgica. O prognóstico para o paciente está diretamente relacionado tanto com o estágio (tamanho do tumor e faixa de crescimento) quanto o grau (as características das células tumorais) do câncer. Tanto o estágio quanto o grau são explicados mais adiante neste capítulo.
Pacientes com CCR de células claras metastático – ou um tumor que se espalhou para outras partes do corpo – apresentam um prognóstico significativamente mais desfavorável.
– Carcinoma de Células Renais (CCR) Papilar
Esta é a segunda forma mais comum de câncer renal, somando aproximadamente 15% dos casos.
O CCR papilar é dividido em dois subtipos com base na aparência celular: Tipo I (5%) e Tipo II (10%). Há um aumento na incidência de CCR papilar em afro-americanos e um aumento na incidência de doença bilateral (envolvendo ambos os rins) associado com este subtipo.
Há também formas hereditárias tanto do CCR papilar Tipo I quanto Tipo II. Quando o CCR papilar não está espalhado, a remoção cirúrgica está geralmente associada a um excelente prognóstico. No entanto, quando ocorre metástase do CCR papilar para outros locais do corpo, a maioria das terapias convencionais para CCR, tal como imunoterapia, são ineficazes.
– Carcinoma de Células Renais (CCR) Cromófobo
Esta forma rara de câncer renal representa aproximadamente 5% dos casos de CCR. Pensa-se que este tipo de CCR se origina a partir do mesmo tipo de célula que aquelas que formam os oncocitomas renais (vide). Tumores híbridos que contém características tanto do CCR cromófobo quanto do oncocitoma renal também foram diagnosticados. Há uma forma familiar ou herdada de CCR cromófobo (em associação com oncocitoma renal) chamada de síndrome de Birt Hogg Dubé, a qual também está associada a uma mutação em um gene específico. Raramente ocorre metástase do CCR cromófobo até tardiamente na sua evolução clínica, e uma remoção cirúrgica de doença localizada ou mesmo localmente avançada está associada, geralmente, a um excelente prognóstico. CCR cromófobo metastático é relativamente raro e nenhuma terapia padrão existe atualmente.
-Carcinoma de Células Renais Não-Classificado
Menos de 1% dos carcinomas de células renais são de tipo não-classificado e são muito raros. Eles não se encaixam em nenhum dos subtipos mais comuns de CCR. Quando examinados em microscópio, estas células de câncer não-classificadas apresentam uma estrutura e características genéticas não compatíveis com a descrição dos subtipos de CCR mais comuns. Esta categoria geralmente inclui tumores agressivos que não respondem à terapia tradicional para CCR.
-Carcinoma dos Ductos Coletores
Esta é uma variação rara e muito agressiva do câncer renal que representa menos de 1% dos casos. Esta forma de CCR é, em geral, metastática no momento do diagnóstico e é mais comum em indivíduos mais jovens. O tratamento foi direcionado no uso de regimes com base em quimioterapia, semelhante àqueles utilizados no tratamento de carcinoma de células transicionais (vide abaixo), uma vez que estes tumores não respondem às terapias tradicionais de CCR, como a bioimunoterapia.
-Carcinoma de Células Renais (CCR) medular
Esta também é uma variação muito rara e agressiva do câncer renal, apesar de ser uma variação do carcinoma dos ductos coletores. Ele está comumente associado ao traço falciforme e, portanto, é mais comum na população afro-americana. Ele representa menos de um por cento dos cânceres renais diagnosticado. A quimioterapia continua sendo o foco principal do tratamento para esta doença.
-Carcinoma de Células Renais (CCR) Sarcomatoide
Esta condição, conhecida como “diferenciação”, pode ocorrer com qualquer um dos subtipos comuns de CCR. O termo se refere ao fato de que as células do CCR – quando visualizadas em microscópio – têm aparência de células de sarcoma. A porcentagem de diferenciação de sarcomatoide é, geralmente, refletida no relato de patologia do tumor e relata a agressividade do tumor. O prognóstico associado ao CCR Sarcomatoide geralmente é desfavorável. A condição é frequentemente encontrada em pacientes cujo câncer renal realizou metástase de forma ampla. Esta forma de câncer renal é, alguma vezes, tratada com quimioterapia.
-Carcinoma de Células Transicionais do Rim (CCT)
Carcinoma de células transicionais (CCT) do rim é um tumor raro e potencialmente muito agressivo que não deve ser considerado um verdadeiro câncer renal, mas ao invés, deve ser agrupado com aqueles cânceres que se desenvolvem a partir da linha do trato urinário. Isto inclui CCT da bexiga, que é muito mais comum do que CCT do rim. Se o câncer não se espalhou, o tumor pode ser tratado por remoção cirúrgica tanto do rim quanto do ureter, embora recorrências de CCT na bexiga sejam comuns. Quando o tumor é grande ou ocorreu metástase, o prognóstico é extremamente desfavorável e as opções de tratamento são semelhantes àquelas para câncer de bexiga metastático, que inclui quimioterapia.
SUBTIPOS
Oncocitoma Renal
Este é um tumor benigno do rim que soma aproximadamente 5% de todos os tumores de rim. Não ocorre metástase destes tumores, embora possam crescer a tal tamanho no rim e invadir estruturas locais, que podem resultar em sintomas que requerem cirurgia. Eles são considerados relacionados ao CCR cromófobo e pode ser muito difícil diferenciar os dois. O tumor é tratado através de remoção parcial ou completa do rim.
A escolha do tratamento, onde o tratamento é feito, a frequência de check-ups e muitos outros aspectos do controle da doença são determinados pelo paciente e o médico. Alguns pacientes acreditam que as informações sobre o câncer renal são apresentadas em termos médicos complicados. Mas, muitas informações, incluindo os recursos recomendados neste guia são especificamente escritos para pacientes em uma linguagem fácil de entender a qual não requer treinamento especializado.
Quanto mais você souber, melhores serão suas decisões, e mais você se sentirá no controle da sua doença. O conhecimento sobre a sua doença o ajudará a se comunicar melhor com seu médico e enfermeira e aumentará sua confiança no tratamento que você recebe. Saber mais sobre o câncer renal é um passo importante para lutar efetivamente contra a doença.
Como prevenir?
NÃO FUMAR → O tabagismo aumenta significativamente o risco do câncer renal. O risco aumentado parece estar relacionado a quantidade que você fuma. O risco cai se você parar de fumar, mas leva muitos anos para se aproximar ao nível de alguém que nunca fumou;
SOBREPESO/OBESIDADE → Manter uma alimentação saúdavel. Abuse de frutas, verduras e legumes. Elas são as maiores fontes de micronutrientes e ajudam na regulação do organismo. As pessoas que estão muito acima do peso apresentam um risco mais alto de desenvolvimento de câncer de células renais. Alguns médicos acreditam que a obesidade é um fator em certa de 2 de 10 pessoas que adquirem este câncer. A obesidade pode provocar alterações em determinados hormônios que podem levar ao carcinoma de células renais;
PRATIQUE EXERCÍCIO FÍSICO → O sobrepeso e a obesidade podem provocar alterações hormonais que levam ao desenvolvimento do câncer;
MODERE NO SAL E REDUZA O AÇÚCAR → evitando a retenção de liquído, alta pressão arterial e diabetes;
BEBA ÁGUA → ela hidrata o organismo e mantém o bom funcionamento dos rins!
Fatores de Risco
Um fator de risco é qualquer coisa que afete suas chances de contrair uma doença, como um câncer. Diferentes tipos de cânceres apresentam diferentes fatores de risco. Por exemplo, a exposição sem proteção a fortes raios solares é um fator de risco para câncer de pele. Mas os fatores de risco não nos dizem tudo. Apresentar um fator de risco, ou mesmo vários fatores de risco, não significa que você terá a doença. E algumas pessoas que adquirem a doença podem não ter apresentado nenhum dos fatores de risco conhecidos. Mesmo se a pessoa com câncer renal apresentar um fator de risco, em geral é muito difícil saber o quanto aquele fator de risco pode ter contribuído para o câncer.
Fatores de risco Genéticos e Hereditários:
Algumas pessoas herdam uma tendência de desenvolver determinados tipos de câncer. O DNA que você herda dos seus pais pode conter determinadas alterações que contribuem para esta tendência de desenvolver câncer. O câncer renal pode ser causado por algumas condições raras herdadas. Pessoas com estas condições apresentam um risco muito mais alto de adquirir câncer renal, embora elas contribuam apenas para uma pequena parte dos casos no total.
Entre os fatores de risco Genéticos e Hereditários estão:
Carcinoma de Células Renais Papilar Hereditário
Pessoas com esta condição apresentam uma tendência herdada de desenvolver um ou mais carcinomas de células renais papilares, porém eles não apresentam tumores em outras partes do corpo, como é o caso de outras condições herdadas listadas aqui. Pensa-se que este distúrbio seja causado por alterações no gene MET.
Doença von Hippel-Lindau
Pessoas com esta condição frequentemente desenvolvem vários tipos de tumores e cistos (bolsas preenchidas por fluídos) em diferentes partes do corpo. Eles apresentam risco aumentado de desenvolver carcinoma de células renais de células claras, especialmente quando mais jovens. Eles também podem apresentar tumores benignos nos olhos, cérebro, medula espinhal, pâncreas e outros órgãos; e um tipo de tumor da glândula suprarrenal chamado feocromocitoma. Esta condição é provocada por mutações (alterações) no gene VHL.
Leiomiomatose Hereditária e Carcinoma de Células Renais
Pessoas com esta síndrome desenvolvem tumores de músculo liso chamados leiomiomas ou fibroides da pele e do útero (em mulheres) e apresentam um risco mais alto de desenvolver cânceres de células renais papilares. Está ligado a alterações no gene da fumarato hidratase (FH).
Síndrome Birt-Hogg-Dube
Pessoas com esta síndrome, que é caracterizada pelo desenvolvimento de pequenos tumores cutâneos benignos, apresentam um risco aumentado de desenvolver diferentes tipos de cânceres de células renais. Eles também podem apresentar tumores benignos ou malignos de vários outros tecidos. O gene ligado a esta condição é conhecido como BHD.
Oncocitoma Renal Hereditário
Algumas pessoas herdam a tendência de desenvolver um tumor de rim chamado oncocitoma, que apresenta um potencial muito baixo de ser maligno. É importante que as pessoas que apresentam causas hereditárias de câncer de células renais visitem seus médicos com frequência, particularmente se elas já têm câncer de células renais diagnosticadas. Alguns médicos recomendam testes de imagem regulares (como exames de CT) para estas pessoas.
Outros
Há alguns fatores de risco que não podem ser alterados, mas podemos aprender a observá-los e relatar qualquer alteração à equipe médica. São eles:
Histórico Familiar de Câncer Renal
As pessoas com um forte histórico familiar de câncer de células renais (sem uma das condições herdadas conhecida listada acima) também apresentam alta chance de desenvolvimento deste câncer. Este risco é ainda mais alto em irmãos (irmãos ou irmãs) daqueles afetados. Se não está claro se é devido à genética, uma exposição ambiental compartilhada, ou alguma combinação destes.
Alta Pressão Arterial
O risco de câncer renal é mais alto em pessoas com alta pressão arterial. Alguns estudos sugeriram que determinados medicamentos utilizados para tratar alta pressão arterial pode desenvolver o risco de câncer renal, mas é difícil dizer se a condição ou a medicação (ou ambos) podem ser a causa do risco aumentado.
Determinados Medicamentos
Fenacetina, um remédio popular para alívio de dor com venda livre, esteve ligado ao câncer de células renais no passado. Alguns estudos sugeriram que diuréticos (medicamentos que tratam a alta pressão arterial provocando que os rins removam o sal e fluído do corpo) podem estar ligados ao carcinoma de células renais. Não está claro se a causa é dos medicamentos ou da alta pressão arterial em si. Se você precisa de diuréticos, você deve tomá-los. Se não precisa, evite-os para tentar reduzir o risco de câncer renal.
Doença de Rim Avançada
Pessoas com doença de rim avançada, especialmente aqueles que precisam de diálise, apresentam um risco mais alto de carcinoma de células renais. A diálise é um tratamento utilizado para remover toxinas do seu corpo caso os rins não funcionem apropriadamente.
Gênero
O carcinoma de células renais e quase duas vezes tão comum em homens quanto em mulheres. Os homens estão provavelmente mais propensos a fumar e a estarem expostos a elementos químicos que provocam câncer no trabalho, que podem contribuir com uma parte da diferença.
Raça
Negros apresentam uma taxa ligeiramente mais alta de câncer de células renais do que brancos. As razões para isto não estão claras.
Sabemos o que causa o câncer renal?
Embora muitos fatores de risco possam elevar sua chance de desenvolver câncer renal, não se sabe ainda de forma exata como alguns desses fatores de risco tornam as células do rim cancerígenas.
Alterações Genéticas
Pesquisadores estão começando a entender como algumas alterações no DNA podem resultar na modificação de células do rim normais em células cancerígenas.
DNA é a molécula química em cada uma de nossas células que compõe nossos genes – as instruções sobre como nossas células funcionam.
Nós geralmente parecemos com os nossos pais porque eles são a fonte de nosso DNA . Contudo, o DNA afeta mais do que nossa aparência.
Alguns genes contêm instruções para controle de quando nossas células devem crescer, se dividir e morrer. Determinados genes que aceleram a divisão celular são chamados oncogenes. Outros genes que diminuem a velocidade da divisão celular ou fazem com que as células morram no momento certo são denominados genes supressores de tumor.
O câncer pode ser causado por mutações do DNA (alterações) que ativam os oncogenes ou desativam os genes supressores de tumor.
Mutações Genéticas Herdadas
Determinadas alterações do DNA herdadas podem levar a condições correntes em algumas famílias que aumentam o risco de câncer renal.
Estas síndromes, que provocam uma pequena parte de todos os cânceres renais, foram descritas na seção Fatores de Risco.
Por exemplo, o gene VHL é um gene supressor de tumor. Ele normalmente ajuda a impedir que as células cresçam fora de controle. As mutações (alterações) neste gene podem ser herdada de um dos pais, provocando a doença von Hippel-Lindau. Quando ocorre mutação no gene VHL, ele não mais suprime o crescimento anormal e é mais provável que o câncer renal se desenvolva.
Os genes ligados à leiomiomatose hereditária, ao carcinoma de células renais (o gene da fumarato hidratase) e à síndrome Birt-Hogg-Dube (o gene BHD) também são genes supressores de tumor, e as alterações herdadas nestes genes também levam a um risco aumentado de câncer renal.
Pessoas com carcinoma de células renais papilar hereditário herdam alterações no oncogene MET que podem provocar que fique “ativo” o tempo todo. Isto torna a pessoa mais propensa a desenvolver câncer de células renais papilar.
Mutações Genéticas Adquiridas
A maioria das mutações de DNA relacionadas ao câncer de mama, entretanto, ocorre durante a vida da pessoa ao invés de ser herdada. Estas mutações adquiridas de oncogenes e/ou dos genes supressores de tumor podem resultar de fatores como exposição a elementos químicos que provocam câncer (como aqueles encontrados no tabaco), porém em muitos casos a causa destas alterações não é conhecida.
Cerca de 3 de 4 pessoas com câncer de células renais claras esporádico (não-herdado) apresentam alterações no gene VHL que provoca que este não funcione apropriadamente. Estas alterações foram adquiridas durante a vida ao invés de serem herdadas.
Outras alterações genéticas também podem provocar carcinomas de células renais. Os pesquisadores continuam a procurar estas alterações.
Algum progresso foi alcançado na compreensão em como o tabaco aumenta o risco de desenvolvimento de carcinoma de células renais. Muitos dos elementos que provocam câncer no tabaco são absorvidos pela corrente sanguínea pelos pulmões. Como os rins filtram este sangue, muitos destes elementos tornam-se altamente concentrados nos rins.
Vários destes elementos químicos são conhecidos por danificar o DNA das células renais de forma que pode tornar células normais em cancerígenas.
A obesidade, outra causa deste câncer, altera o equilíbrio de alguns dos hormônios do corpo. Os pesquisadores estão agora aprendendo como determinados hormônios ajudam a controlar o crescimento (tanto normal quanto anormal) de muitos tecidos diferentes no corpo, incluindo os rins.
Conhecimento das alterações genéticas que podem levar ao câncer de mama está sendo utilizado para ajudar a desenvolver novos tratamentos para esta doença. Por exemplo, os pesquisadores agora sabem que o gene VHL normalmente impede que as células produzam uma substância chamada fator do crescimento endotelial vascular (VEGF). Esta substância provoca a formação de novos vasos sanguíneos, dos quais os tumores precisam para sobreviver e crescer. Medicamentos recentes que têm como alvo o VEGF estão agora sendo utilizados para tratar o câncer renal.
Alguns possíveis sinais e sintomas de câncer renal incluem:
> sangue na urina (hematúria);
> dor lombar em um lado (não provocada por lesão);
> uma massa ou inchaço no lado ou na região lombar;
> fadiga;
> perda de peso não explicada;
> febre que não é causada por um resfriado ou outra infecção e que não passa após poucas semanas;
> inchaço dos tornozelos e pernas (edema);
Estes sintomas podem ser causados pelo câncer, mas com mais frequência se dão devido a doenças não-cancerosas. Por exemplo, sangue na urina pode ser um sinal de câncer renal, bexiga ou de próstata, mas com muita frequência é provocado por infecção na bexiga ou pedra no rim. Ainda, se você apresentar algum destes sintomas, consulte um médico, assim a causa pode ser avaliada e tratada, se necessário.
Como o Câncer Renal é Diagnosticado?
Muitos cânceres renais são encontrados regularmente de forma precoce, enquanto eles ainda estão confinados no rim. Porém, outros são encontrados em um estágio mais avançado. Há algumas razões para isto:
> Estes cânceres podem, algumas vezes, se tornar muito grandes sem provocar nenhuma dor ou outros problemas;
> Devido ao fato do rim estar muito adentro do corpo, pequenos tumores do rim não podem ser observados ou sentidos durante um exame físico;
> Não há testes simples que possam ser utilizados para examinar o câncer renal em pessoas que não estão em risco aumentado.
Um teste de urina de rotina, que, às vezes, é parte de um exame médico completo, pode encontrar pequenas quantidades de sangue na urina de algumas pessoas com câncer de células renais precoce. Porém, há muitas outras causas de sangue na urina, incluindo infecções do trato urinário, infecções da bexiga, câncer da bexiga e condições benignas do rim (não cancerosas), tais como pedras no rim.
Por outro lado, algumas pessoas com câncer renal não apresentam sangue na urina até que o câncer esteja muito grande e possa ter se espalhado para outras partes do corpo. Exames de imagem, tais como exames de tomografia computadorizada (CT) e exames de imagem por ressonância magnética (MRI) podem encontrar pequenos carcinomas de células renais. Mas estes exames são caros e nem sempre revelam tumores benignos de pequenos carcinomas de células renais. Por estas razões, os médicos geralmente recomendam CT e MRI para detecção precoce de câncer renal apenas em pessoas que apresentam determinados fatores de risco, tais como doença von Hippel-Lindau (VHL) ou outras condições herdadas. Alguns médicos também recomendam que pessoas com doenças de rim tratadas por diálise em longo prazo realizem testes periódicos (exames de CT ou MRI) para procurar por câncer renal. Em geral, cânceres renais são encontrados incidentalmente durante exames para algumas outras doenças, tais como doença de vesícula biliar. Estes cânceres geralmente não provocam dor ou desconforto no momento da descoberta. A taxa de sobrevida para câncer renal descoberto desta forma é muito alta, pois estes cânceres geralmente são descobertos em um estágio muito precoce.
Saiba mais sobre diagnóstico precoce:
É importante dizer ao seu médico se familiares (parentes de sangue) apresentam ou apresentaram câncer renal, especialmente quando jovens, ou se eles foram diagnosticados com uma condição herdada ligada a este câncer, como doença VHL. Seu médico pode recomendar que você considere o teste genético. O teste genético para estas condições é utilizado apenas em pessoas com sinais clínicos destas condições e em seus parentes de sangue. Antes de realizar os testes genéticos, é importante falar com um consultor genético, assim você entende o que os testes podem – e não podem – dizer a você, e o que alguns resultados significariam. Os testes genéticos procuram mutações genéticas que provocam estas condições no seu DNA. Eles são utilizados para diagnosticar estas condições herdadas, não o câncer renal em si. Seu risco pode estar aumentado se você apresentar uma destas condições, mas isto não significa que você apresenta (ou definitivamente apresentará) câncer renal. Se você foi diagnosticado com uma destas condições, você pode precisar de frequentes exames de CT ou MRI para procurar por câncer renal.
Para o dignóstico do câncer renal são utilizados exames de imagem e laboratóriais. Abaixo listados os exames necessários para diagnosticar o câncer renal:
Exames de Imagem
Exames por imagem utilizam raios-X, campos magnéticos ou substâncias radioativas para criar fotos de dentro do seu corpo. Exames de imagem podem ser realizados por um número de motivos, incluindo ajudar a descobrir se a área suspeita pode ser cancerosa, saber o quão longe o câncer pode ter se espalhado e ajudar a determinar se o tratamento foi eficaz. Diferente da maioria dos outros cânceres, os médicos podem com frequência ter certeza sobre o diagnóstico do câncer renal sem precisar realizar uma biópsia (remoção de uma amostra do tumor para ser observado em microscópio). Em muitos casos, os exames de imagem podem dar aos médicos uma quantidade razoável de certeza que uma massa do rim é (ou não) cancerosa. Em alguns casos, no entanto, uma biópsia pode ser necessária para ter certeza. Exames de tomografia computadorizada (CT), exames de imagem por ressonância magnética (MRI), pielogramas intravenosos e ultrassom podem ser muito úteis no diagnóstico na maioria dos tipos de tumores renais, embora os pacientes raramente precisem de todos estes exames. Outros exames descritos aqui, como raios-X do tórax e exames ósseos são utilizados com mais frequência para ajudar a determinar se o câncer se propagou (ocorreu metástase) para outras partes do corpo.
Exame de Tomografia Computadorizada (CT ou CAT)
O exame de Exame de Tomografia Computadorizada (CT ou CAT) consiste em um exame de raio-X que produz imagens seccionais cruzadas detalhadas do seu corpo. Ao invés de tirar uma fotografia, como um raio-X convencional, o aparelho de CT obtém diversas imagens conforme gira ao seu redor, enquanto você está deitado em uma mesa. Então, um computador combina essas imagens na forma de imagens de fatias da parte do corpo que está sendo estudada. Diferente de um raio-X convencional, um exame de CT cria imagens detalhadas dos tecidos moles no corpo. Depois de obtido o primeiro grupo de imagens, pode ser solicitado que você beba uma solução de contraste e/ou você pode receber um cateter IV (intravenoso) por meio do qual é injetado um corante de contraste. Ele ajuda a delinear melhor as estruturas do seu corpo. Em seguida, se obtém um segundo grupo de imagens.
O contraste pode provocar um pouco de rubor (uma sensação de calor, especialmente na face). Algumas pessoas são alérgicas e apresentam urticária. Raramente, podem ocorrer reações mais sérias como dificuldades para respirar ou queda da pressão arterial. Não deixe de informar o médico caso você sofra ou já tenha sofrido alguma reação a qualquer material de contraste utilizado para raios-X.
Exames de CT são mais demorados do que raios-X convencionais. Você precisa ficar deitado em uma mesa durante sua realização. Durante o exame, a mesa se movimenta para dentro e para fora do aparelho, uma máquina em formato de anel que envolve completamente a mesa. Você pode se sentir um pouco confinado pelo anel em que deve se deitar enquanto as imagens são obtidas.
Nos últimos anos, a CT espiral (também conhecida como CT helicoidal) se tornou disponível em muitos centros médicos. Este tipo de exame de CT utiliza uma máquina mais rápida. A parte da máquina que obtém a imagem roda em volta do corpo continuadamente, permitindo que os médicos coletem as imagens mais rapidamente do que com a CT padrão. Isto reduz a chance de imagens “borradas” decorrentes do movimento de respiração. Também diminui a dose de radiação recebida durante o exame. A maior vantagem pode ser que as “fatias” de imagem que ele obtém são mais finas, o que proporciona imagens mais detalhadas e permite que médicos olhem as áreas suspeitas de diferentes ângulos.
O exame de CT é um dos exames mais úteis para achar e olhar uma massa dentro do rim. Ele também é útil para verificar se um câncer se espalhou, ou não, para órgãos e tecidos além do rim. O exame de CT fornecerá informações precisas sobre o tamanho, formato e posição de um tumor, e pode ajudar a encontrar linfonodos maiores que possam conter câncer.
Imagem por Ressonância Magnética (MRI)
Assim como os exames de Tomografia Computadorizada (CT), os exames de Imagem por Ressonância Magnética (MRI) fornecem imagens detalhadas de tecidos moles no corpo.
Exames de MRI são utilizados com menos frequência do que os exames de CT em pessoas com câncer renal. Eles podem ser realizados em casos onde os exames de CT não são práticos, tais como se a pessoa for alérgica ao contraste de CT.
Exames de MRI também podem ser realizados se houver uma chance do câncer envolver uma veia principal no abdômen (veia cava inferior). Finalmente, eles podem ser utilizados para procurar possível propagação do câncer para o cérebro ou para a medula espinhal se uma pessoa apresentar sintomas que sugerem que este possa ser o caso.
Ultrassom (ultrassonografia ou US)
O ultrassom utiliza ondas sonoras para criar imagens de órgãos internos.
Para este exame, um pequeno instrumento semelhante a um microfone chamado transdutor é colocado na pele próximo ao rim. Ele emite ondas sonoras e capta os ecos conforme eles são refletidos pelos tecidos no rim. Os ecos são convertidos por um computador em uma imagem em preto e branco que é exibida em uma tela de computador. Este exame é indolor e não expõe você à radiação.
O ultrassom pode ser útil para determinar se uma massa do rim é sólida ou preenchida por fluído. Os modelos de eco produzidos pela maioria dos tumores do rim parecem diferentes daqueles do tecido do rim normal.
Diferentes modelos de eco também podem distinguir alguns tipos de tumores benignos e malignos do rim um do outro. Se uma biópsia de rim for necessária, este exame pode ser utilizado para guiar uma agulha da biópsia na massa para obter uma amostra.
Exame de Tomografia por Emissão de Pósitron (PET SCAN)
Exames de PET SCAN envolvem a injeção de uma forma de açúcar radioativo (conhecido como fluorodeoxiglicose ou FDG) no sangue. A quantidade de radioatividade utilizada é muito baixa.
Como as células cancerosas do corpo crescem rapidamente, elas absorvem grandes quantidades do açúcar radioativo. Uma câmera especial pode, assim, gerar uma imagem de áreas de radioatividade do corpo. A imagem não é extremamente detalhada como um exame de CT ou MRI, mas proporciona informações úteis sobre o corpo todo.
Este exame pode ser útil para observar se o câncer pode ter se espalhado para os linfonodos próximos ao rim. Exames de PET também podem ser úteis quando o médico acredita que o câncer possa ter se espalhado, mas não tem conhecimento de onde isso ocorreu. Exames de PET podem ser utilizados ao invés de diversos raios-X diferentes, pois eles realizam varredura do corpo inteiro.
Algumas máquinas mais recentes conseguem realizar tanto um exame de PET quanto um exame de CT ao mesmo tempo (exame PET/CT). Isso permite ao radiologista comparar áreas de maior radioatividade no PET com a aparência da mesma área na CT.
Pielograma Intravenoso (IVP)
Um pielograma intravenoso é um raio-X do sistema urinário realizado após um corante especial ter sido injetado na veia. Este corante sai da corrente sanguínea para os rins e, então, passa pelos ureteres e bexiga.
Um IVP pode ser útil para encontrar anormalidades do trato urinário, tais como câncer, mas você pode não precisar de um IVP caso já tenha realizado uma CT ou MRI.
Angiografia
Assim como IVP, este exame de raio-X também utiliza um corante de contraste. Um cateter é geralmente preso a uma artéria de grande porte na sua perna na artéria que segue para o rim (artéria renal). O corante é, então, injetado na artéria para contornar os vasos sanguíneos.
Como a angiografia pode contornar os vasos sanguíneos que alimentam o tumor do rim, ela pode ajudar o cirurgião a planejar uma cirurgia. A angiografia também pode ajudar a diagnosticar cânceres renais uma vez que os vasos sanguíneos geralmente apresentam uma aparência especial com este exame.
Raio-X do Tórax
Se o câncer renal foi diagnosticado (ou há suspeita), um raio-X plano do seu tórax pode ser realizado para observar se o câncer se propagou para os pulmões. Isto é muito improvável, a menos que o câncer esteja muito avançado. Este raio-X pode ser realizado em qualquer contexto ambulatorial. Se os resultados forem normais, provavelmente você não apresenta câncer nos pulmões.
Exame Ósseo
Um exame ósseo pode ajudar a mostrar se o câncer sofreu metástase (se espalhou) para os ossos. Nesse exame, é injetada uma pequena quantidade de material de baixo nível de radioatividade em uma veia (por via intravenosa, ou IV). A substância se deposita nas áreas do osso comprometido por todo o esqueleto, no decorrer de algumas horas. Então, você fica deitado sobre uma mesa por cerca de 30 minutos enquanto uma câmera especial detecta a radioatividade e gera uma imagem do seu esqueleto.
Áreas de alterações ósseas ativas como “hot spots” no seu esqueleto – ou seja, elas atraem a radioatividade. Essas áreas podem sugerir a presença de câncer metastático, no entanto, a artrite e outras doenças ósseas também podem produzir o mesmo padrão. Para distinguir entre essas condições, sua equipe de cuidados oncológicos pode utilizar outros exames de imagem, como raios-x simples ou exames de CT e MRI, para conseguir uma visualização melhor das áreas realçadas, ou podem até mesmo colher amostras do osso para biópsia.
Exames ósseos são realizados principalmente quando há motivo para pensar que o câncer possa ter se espalhado para os ossos (pois uma pessoa apresenta sintomas como dor óssea). Exames de PET geralmente também podem mostrar a propagação do câncer para os ossos, portanto, se você realizou um exame de PET você pode não precisar de um exame ósseo.
Exames Laboratoriais
Exames laboratoriais geralmente não são utilizados para diagnosticar câncer renal, mas eles podem, algumas vezes, dar a primeira pista de que pode haver um problema com os rins. Eles também são realizados para ter uma ideia da saúde geral da pessoa e para ajudar a dizer se o câncer pode ter se espalhado para outras áreas. Antes da cirurgia, eles podem ajudar a dizer se uma pessoa é saudável o suficiente para realizar a operação.
Exame de Urina (Urinálise)
O Exame de Urina (Urinálise) é, algumas vezes, parte de um exame físico completo, mas ele pode não ser realizado como parte de exames físicos de rotina. É provável que seja um dos primeiros exames realizados caso o câncer renal seja uma possibilidade.
Exames microscópicos e químicos são realizados na urina para procurar pequenas quantidades de sangue e outras substâncias não observadas a olho nu. Cerca de metade dos pacientes com câncer de células renais apresentam sangue na urina. Algumas vezes, exame microscópico especial de amostras da urina (chamado citologia da urina) mostrará células cancerosas reais na urina.
Hemograma
O hemograma pode detectar achados algumas vezes observados com câncer de células renais. Anemia (pouquíssimos eritrócitos) é muito comum. Com menos frequência, uma pessoa pode apresentar muitos eritrócitos, pois o câncer renal produz um hormônio (eritropoietina) que provoca que a medula óssea produza mais eritrócitos. As contagens de sangue também são importantes para se certificar que uma pessoa é saudável o suficiente para uma cirurgia.
Exames de Bioquímica do Sangue
Exames de bioquímica do sangue geralmente são realizados em pessoas que possam apresentar câncer renal, uma vez que ele pode afetar os níveis de determinados elementos químicos no sangue. Por exemplo, altos níveis de enzimas hepáticas são encontrados algumas vezes, embora os motivos para isso não sejam conhecidos. Altos níveis de cálcio no sangue podem indicar que o câncer se espalhou para os ossos e pode, portanto, alertar o médico para solicitar um exame ósseo.
Biópsia por Aspiração com Agulha Fina
Este exame é raramente utilizado para diagnosticar tumores de rim. Estudos por imagem geralmente fornecem informações suficientes para um cirurgião decidir se a operação é ou não necessária. Algumas vezes a biópsia por aspiração com agulha fina (FNA) é utilizada para obter pequena amostra das células de uma área suspeita se os resultados do exame de imagem não forem conclusivos o suficiente para garantir a remoção do rim. Ela também pode ser realizada para confirmar o diagnóstico de câncer se a saúde da pessoal for muito deficiente para cirurgia e outros tratamentos locais (tais como embolização arterial ou crioterapia) estão sendo considerados. Para este exame, a pele onde a agulha será inserida é, em primeiro lugar, adormecida com anestesia local. O médico direciona uma agulha vazia na área enquanto observa seu rim com exames de ultrassom ou CT. Diferente do ultrassom, a CT não fornece uma imagem contínua, então a agulha é inserida na direção da massa, uma imagem de CT é obtida e a direção da agulha é orientada com base na imagem. Isto é repetido algumas vezes até a agulha estar dentro da massa. Uma pequena amostra da área-alvo é sugada (aspirada) para uma seringa e observada em microscópio para observar se células cancerosas estão presentes. Em casos onde os médicos pensam que o câncer renal possa ter se espalhado para outros locais, eles podem realizar uma biópsia do local metastático ao invés do rim.
Grau de Fuhrman
O grau de Fuhrman é determinado pela observação das células do câncer renal (obtidas durante uma biópsia ou durante cirurgia) em um microscópio. Ele é utilizado por muitos médicos como uma maneira de descrever o quão agressivo o câncer provavelmente pode ser. O grau é baseado em o quanto os núcleos das células cancerosas (parte de uma célula na qual o DNA é armazenado) se parece com aqueles de células de um rim normal. Os cânceres de células renais geralmente são graduados em uma escala de 1 até 4. Os cânceres de células renais grau 1 têm núcleos celulares que diferem muito pouco dos núcleos celulares de um rim normal. Estes cânceres normalmente crescem e se espalham lentamente e tendem a apresentar uma boa perspectiva. No outro extremo, núcleos de câncer de células renais grau 4 são muito diferentes de núcleos de células de um rim normal e apresentam um pior prognóstico. Embora o tipo celular e o grau algumas vezes sejam úteis na previsão do prognóstico, o estágio do câncer está longe de ser a melhor previsão de sobrevida. O estágio descreve o tamanho do câncer e o quanto ele se espalhou além do rim.
Como é tratado?
O tratamento varia de pessoa para pessoa. A escolha depende muito do estágio do câncer, do estilo de vida do paciente e da alimentação. Após a determinação do câncer e de seu estágio, a equipe de cuidados oncológicos discutirá com o paciente as opções de tratamento. No caso do câncer renal, as opções de tratamento podem incluir cirurgia, terapia por radiação, terapia-alvo, imunoterapia, quimioterapia ou outras dessas combinações, dependendo dos fatores acima mencionados.
Tipos de Tratamento
Cirurgia
A cirurgia é o principal tratamento para a maioria dos carcinomas de células renais. As chances de sobreviver a um câncer de célula renal sem cirurgia são pequenas. Dependendo do estágio e do local do câncer e outros fatores, a cirurgia pode ser usada para remover tanto o câncer com alguns tecidos circundantes do rim quanto o rim em sua totalidade.
Radioterapia
A Radioterapia usa radiação de alta energia para matar as células cancerígenas. A terapia por feixe externo foca a radiação a partir do lado de fora do corpo sob o câncer. É como fazer um raio-x, mas a radiação é muito mais intensa. O procedimento em si é indolor. A radioterapia pode ser usada para tratar o câncer renal se a saúde geral da pessoa estiver muito debilitada para passar por cirurgia. Infelizmente, os cânceres renais não são muito sensíveis à radiação. Usar radioterapia antes ou após a remoção do câncer, não é rotineiramente recomendado porque os estudos não mostraram que ela melhora as taxa de sobrevida.
Quimioterapia
Quimioterapia usa medicamentos anticâncer que são administrados na veia ou pela boca (em forma de pílulas). Esses medicamentos entram na corrente sanguínea e alcançam todas as áreas do corpo, o que torna o tratamento potencialmente útil para o câncer que se disseminou (metastatizado) para os órgãos além dos rins.Infelizmente, as células do câncer renal são geralmente resistentes à quimioterapia, e não existe nenhuma maneira padrão de tratá-las com esses medicamentos. A quimioterapia é geralmente reservada para cânceres onde os medicamentos alvo e/ou imunoterapia não são eficazes.
Terapia-alvo
A terapia alvo é considerada uma medida terapêutica que veio revolucionar o tratamento do câncer, causando menos danos às células sadias. Utilizam anticorpos monoclonais, capazes de limitar o crescimento do tumor, em uma ação semelhante ao nosso sistema imunológico. Cerca de 20 a 25% dos casos se beneficiam dessa alternativa.
Imunoterapia
Segundo o Instituto Nacional do Câncer – INCA, é chamado de imunoterapia o tratamento do câncer que promove a estimulação do sistema imunológico, por meio do uso de substâncias modificadoras da resposta biológica. A imunoterapia é classificada em ativa e passiva, de acordo com as substâncias utilizadas e os seus mecanismos de ação. Na imunoterapia ativa, substâncias estimulantes e restauradoras da função imunológica (imunoterapia inespecífica) e as vacinas de células tumorais (imunoterapia específica) são administradas com a finalidade de intensificar a resistência ao crescimento tumoral. Na imunoterapia passiva ou adotiva, anticorpos antitumorais ou células mononucleares exógenas são administradas, objetivando proporcionar capacidade imunológica de combate a doença.
Curiosidades sobre o câncer renal:
- Você sabe a quantidade ideal que você deve consumir de água por dia? Saiba que cada pessoa possui uma quantidade ideal. Descubra qual a sua no site do Instituto Espaço de Vida e comece agora a beber a sua quantidade ideal!
- Voce sabe quanto pesa o seu rim? 150 gramas é o peso de cada um dos seus rins.
- Os cálculos Renais aumentam cerca de 30% durante o verão. Por isso, fique atento!
Como o Câncer Renal é Classificado?
O estadiamento é o processo de descobrir o quanto o câncer se espalhou. Seu tratamento e prognóstico (a previsão de chances de sobrevida) dependem, em grande parte, do estágio do câncer.
O estadiamento está baseado em resultados de exame físico, biópsias e exames de imagem (exame de CT, raio-X do tórax, exame de PET, etc.).
Na verdade, há 2 tipos de estadiamento para o câncer renal. O estágio clínico é a melhor estimativa do seu médico da extensão da sua doença, com base nos resultados de exame físico, exames laboratoriais e qualquer estudo de imagem que você tenha realizado. Se você realizar cirurgia, seus médicos também podem determinar o estágio patológico, que é baseado em alguns fatores como estágio clínico, mais o que for encontrado durante a cirurgia e exame do tecido removido. Isto significa que se você realizar uma cirurgia, o estágio do câncer pode realmente mudar depois disso (se foi descoberto que o câncer se espalhou mais do que estava suspeito, por exemplo). Provavelmente, o estadiamento patológico é mais preciso que o clínico, já que permite ao médico obter uma impressão direta da extensão do câncer.
Sistema de Estadiamento AJCC (TNM)
O sistema de estadiamento é uma maneira padronizada no qual a equipe de tratamento oncológico descreve a extensão do câncer. O sistema de estadiamento mais comumente utilizado é o da American Joint Committee on Cancer (Comitê da Junta Americana do Câncer) (AJCC), algumas vezes também conhecido como sistema TNM. O sistema TNM descreve 3 informações-chave:
> T indica o tamanho do tumor principal (primário) e se ele cresceu para as áreas próximas.
> N descreve a extensão de propagação para os linfonodos próximos (regionais). Os linfonodos são pequenos grupos de células do sistema imune em formato de feijão que são importantes na luta contra infecções.
> M indica se o câncer se espalhou (sofreu metástase) para outros órgãos do corpo. (Os locais mais comuns de propagação são para os pulmões, ossos, fígado e linfonodos distantes).
Números ou letras aparecem após T, N e M para fornecer mais detalhes sobre cada um destes fatores. Os números 0 a 4 indicam gravidade crescente. A letra X significa “não pôde ser avaliado, pois as informações não estavam disponíveis”.
Categorias T para Câncer Renal
TX: O tumor primário não pode ser avaliado (informações não disponíveis).
T0: Nenhuma evidência de tumor primário.
T1a: O tumor mede 4 cm (cerca de 11/2 polegadas) em sua extremidade ou é menor e está limitado ao rim.
T1b: O tumor mede mais que 4 cm, mas não maior que 7 cm (cerca de 2 ¾ polegadas) em sua extremidade e ainda está limitado ao rim.
T2: O tumor mede mais que 7 cm em sua extremidade mas ainda é limitado ao rim.
T3a: O tumor se espalhou pela glândula suprarrenal (que está situada sobre o rim) ou dentro do tecido adiposo ao redor do rim, mas não para além da camada fibrosa que circunda o rim e as proximidades do tecido adiposo (Fáscia de Gerota).
T3b: O tumor se espalhou para dentro da veia principal que leva para fora do rim (veia renal) e/ou a parte da maior veia que leva para o coração (veia cava) que está dentro do abdome.
T3c: O tumor atingiu a parte da veia cava que está dentro do tórax ou invadiu a parede da veia cava.
T4: O tumor se espalhou para além da fáscia de Gerota (camada fibrosa ao redor do rim e próximo do tecido adiposo).
Categorias N para Câncer Renal
NX: Os linfonodos regionais (proximidades) não podem ser avaliados (informação não disponível).
N0: Não se espalhou nos arredores dos linfonodos.
N1: Espalhou-se para os arredores de 1 linfonodo.
N2: Espalhou-se para os arredores de mais de 1 linfonodo.
Categorias M para Câncer Renal
MX: A presença de metástase distante não pode ser avaliada (informação não disponível).
M0: Não se espalhou para os linfonodos distantes ou outros órgãos.
M1: Presença de metástase distante; inclui a propagação para os linfonodos distantes e/ou para outros órgãos (tais como pulmões, ossos ou cérebro).
Grupamento por Estágio
Uma vez que as categorias T, N e M foram determinadas, esta informação é combinada para determinar o estágio global de I, II, III ou IV. O estágio identifica cânceres que apresentam um prognóstico semelhante, e portanto, são tratados de maneira semelhante. Os pacientes com estágio de menor número tendem a apresentar prognósticos melhores.
Estágio I
T1a-T1b, N0, M0: O Tumor mede 7 cm ou menos e é limitado ao rim. Não há disseminação para os linfonodos ou órgãos distantes.
Estágio II
T2, N0, M0: O tumor mede mais que 7 cm, mas ainda é limitado ao rim. Não há disseminação para os linfonodos ou órgãos distantes.
Estágio III
Diferentes combinações de categorias T e N são incluídas neste estágio.
T3a-T3c, N0, M0: O tumor principal atingiu a glândula suprarrenal, o tecido adiposo ao redor do rim, a veia renal e/ou a veia principal (veia cava) levando do rim ao coração. Ele não se espalhou para além da fáscia de Gerota. Não há disseminação para os linfonodos ou órgãos distantes.
T1a-T3c, N1, M0: O tumor principal pode ser de qualquer tamanho e pode estar fora do rim, mas não se espalhou para além da fáscia de Gerota. O câncer se espalhou para os arredores de 1 linfonodo mas não se espalhou para os linfonodos distantes ou outros órgãos.
Estágio IV
Existem diversas combinações de categorias T, N e M que estão incluídas neste estágio.
T4, N0-N1, M0: O tumor principal invadiu além da fáscia de Gerota. Espalhou-se para os arredores de mais de 1 linfonodo. Não se espalhou para os linfonodos distantes ou outros órgãos.
Qualquer T, N2, M0: O tumor principal pode ter qualquer tamanho e pode estar fora do rim. O câncer se espalhou para os arredores de mais de 1 linfonodo mas não se espalhou para os linfonodos distantes ou outros órgãos.
Qualquer T, Qualquer N, M1: O tumor principal pode ter qualquer tamanho e pode estar fora do rim. Pode ter se espalhado ou não para perto dos linfonodos. Espalhou-se para os linfonodos distantes e/ou outros órgãos.
Outros Sistemas
Embora o sistema de classificação TNM seja útil, alguns médicos têm apontado que existem outros fatores além da extensão do câncer que devem ser considerados na determinação do prognóstico e tratamento.
Universidade da Califórnia em Los Angeles (UCLA) Sistema de Classificação Integrado
Este é um sistema mais complexo porém provavelmente mais preciso. Junto com o estágio do câncer, leva em consideração a saúde global da pessoa e o grau de Fuhrman do tumor para dividir pessoas em grupos de risco baixo, intermediário e alto. Você pode querer perguntar ao seu médico se ele ou ela usa este sistema e como ele pode se aplicar ao seu caso.
- O que é?
-
Atualmente, o câncer renal, representa cerca de 3% das doenças malignas em adultos no mundo. No Brasil, surgiu mais de 580 mil casos novos até o final de 2015, sendo duas vezes mais frequente nos homens que nas mulheres. O tipo mais comum do câncer renal é o carcinoma de células renais, que representa 90% dos casos, e se origina nos rins, podendo se espalhar pelo corpo. Dados publicados pelo Globocan, um projeto da Organização Mundial da Saúde que visa coletar, organizar e divulgar dados estimativos da incidência e mortalidade dos tipos mais comuns de câncer no mundo, apontam que, em 2015, 6.768 pessoas receberam o diagnóstico de câncer de rim no Brasil, sendo 4.068 homens e 2.700 mulheres. A maioria das pessoas com câncer renal são mais velhas. A idade média das pessoas quando diagnosticadas é de 65 anos. O câncer de rim é muito raro em pessoas com menos de 45 anos de idade. Ele está entre os 10 tipos de cânceres mais comuns em homens e mulheres. No geral, o risco de desenvolver câncer de rim é cerca de 1 em 63 (1,6%).
Sobre os Rins:
Os rins são um par de órgãos em formato de um feijão. Um rim está localizado do lado esquerdo e o outro do lado direito da coluna vertebral. Ambos estão protegidos pela caixa torácica. A principal função dos rins é filtrar o sangue e remover do corpo o excesso de água, sal e produtos residuais. Os produtos residuais filtrados são concentrados na urina. Os rins também ajudam a verificar se o corpo tem eritrócitos (também conhecidos como glóbulos vermelhos ou hemácias) suficientes. Os rins também atuam secretando substâncias importantes para nossa saúde. Entre suas funções, pode-se destacar a manutenção do equilíbrio de eletrólitos no corpo, como sódio, potássio, cálcio, magnésio, fósforo, bicarbonato etc.; a regulação do equilíbrio ácido-básico, mantendo o pH sanguíneo constante; a excreção de substâncias exógenas, como medicações; e a produção de hormônios, como aldosterona e prostaglandinas.
O câncer de rim é também conhecido como hipernefroma ou adenocarcinoma renal. Existem vários tipos de câncer renal. O mais frequente é o câncer renal de células claras, sendo responsável por 85% dos tumores diagnosticados. Entenda sobre o Câncer Renal de Células Claras: O CCR de célula clara é o tipo de célula associado com a mutação no gene von Hippel Lindau (VHL) no câncer renal hereditário. De fato, aproximadamente 70% dos casos não hereditários de CCR de células claras também apresentam mutação no aVHL.
Conheça os Tipos de Câncer Renal:
– Carcinoma de Células Renais (CCR)
Nem todos os cânceres renais são os mesmos. Há um crescente entendimento entre os médicos e pesquisadores de que há diferentes subtipos de CCR e que eles se comportam de formas completamente diferentes, tanto com relação ao quanto são agressivos no paciente quanto como eles respondem ao tratamento. Há dez ou quinze anos, era comum para um relato de patologia de um paciente com câncer renal se ler simplesmente Carcinoma de Células Renais. Hoje, este diagnóstico simples é considerado incompleto. A identificação do subtipo específico ou tipo de célula (histologia) do câncer renal pode ser tão importante na determinação do prognóstico do paciente quanto saber o estágio e o grau do CCR. Seu médico deve lhe oferecer informações sobre a histologia, grau e estágio do seu câncer renal. Em caso negativo, você deve se sentir confortável em pedir estas informações uma vez que é uma parte importante do seu planejamento de tratamento.
Os subtipos de CCR vêm da descrição da aparência das células e outras características. Eles incluem:– Carcinoma de Células Renais (CCR) de Células Claras
Esta é a forma mais comum de câncer renal e representa entre 66% e 75% de todos os casos. O CCR de célula clara é o tipo de célula associado com a mutação no gene von Hippel Lindau (VHL) no câncer renal hereditário. De fato, aproximadamente 70% dos casos não hereditários de CCR de células claras também apresentam mutação no aVHL. Muito da pesquisa atual, que tenta identificar novos tratamentos efetivos para pacientes com doença localmente avançada ou metastática, foca neste subtipo da doença, uma vez que é o tipo mais comum de CCR.
Quando o tumor não está espalhado, o prognóstico é muito bom depois de excisão cirúrgica. O prognóstico para o paciente está diretamente relacionado tanto com o estágio (tamanho do tumor e faixa de crescimento) quanto o grau (as características das células tumorais) do câncer. Tanto o estágio quanto o grau são explicados mais adiante neste capítulo.
Pacientes com CCR de células claras metastático – ou um tumor que se espalhou para outras partes do corpo – apresentam um prognóstico significativamente mais desfavorável.
– Carcinoma de Células Renais (CCR) Papilar
Esta é a segunda forma mais comum de câncer renal, somando aproximadamente 15% dos casos.
O CCR papilar é dividido em dois subtipos com base na aparência celular: Tipo I (5%) e Tipo II (10%). Há um aumento na incidência de CCR papilar em afro-americanos e um aumento na incidência de doença bilateral (envolvendo ambos os rins) associado com este subtipo.
Há também formas hereditárias tanto do CCR papilar Tipo I quanto Tipo II. Quando o CCR papilar não está espalhado, a remoção cirúrgica está geralmente associada a um excelente prognóstico. No entanto, quando ocorre metástase do CCR papilar para outros locais do corpo, a maioria das terapias convencionais para CCR, tal como imunoterapia, são ineficazes.
– Carcinoma de Células Renais (CCR) Cromófobo
Esta forma rara de câncer renal representa aproximadamente 5% dos casos de CCR. Pensa-se que este tipo de CCR se origina a partir do mesmo tipo de célula que aquelas que formam os oncocitomas renais (vide). Tumores híbridos que contém características tanto do CCR cromófobo quanto do oncocitoma renal também foram diagnosticados. Há uma forma familiar ou herdada de CCR cromófobo (em associação com oncocitoma renal) chamada de síndrome de Birt Hogg Dubé, a qual também está associada a uma mutação em um gene específico. Raramente ocorre metástase do CCR cromófobo até tardiamente na sua evolução clínica, e uma remoção cirúrgica de doença localizada ou mesmo localmente avançada está associada, geralmente, a um excelente prognóstico. CCR cromófobo metastático é relativamente raro e nenhuma terapia padrão existe atualmente.
-Carcinoma de Células Renais Não-Classificado
Menos de 1% dos carcinomas de células renais são de tipo não-classificado e são muito raros. Eles não se encaixam em nenhum dos subtipos mais comuns de CCR. Quando examinados em microscópio, estas células de câncer não-classificadas apresentam uma estrutura e características genéticas não compatíveis com a descrição dos subtipos de CCR mais comuns. Esta categoria geralmente inclui tumores agressivos que não respondem à terapia tradicional para CCR.
-Carcinoma dos Ductos Coletores
Esta é uma variação rara e muito agressiva do câncer renal que representa menos de 1% dos casos. Esta forma de CCR é, em geral, metastática no momento do diagnóstico e é mais comum em indivíduos mais jovens. O tratamento foi direcionado no uso de regimes com base em quimioterapia, semelhante àqueles utilizados no tratamento de carcinoma de células transicionais (vide abaixo), uma vez que estes tumores não respondem às terapias tradicionais de CCR, como a bioimunoterapia.
-Carcinoma de Células Renais (CCR) medular
Esta também é uma variação muito rara e agressiva do câncer renal, apesar de ser uma variação do carcinoma dos ductos coletores. Ele está comumente associado ao traço falciforme e, portanto, é mais comum na população afro-americana. Ele representa menos de um por cento dos cânceres renais diagnosticado. A quimioterapia continua sendo o foco principal do tratamento para esta doença.
-Carcinoma de Células Renais (CCR) Sarcomatoide
Esta condição, conhecida como “diferenciação”, pode ocorrer com qualquer um dos subtipos comuns de CCR. O termo se refere ao fato de que as células do CCR – quando visualizadas em microscópio – têm aparência de células de sarcoma. A porcentagem de diferenciação de sarcomatoide é, geralmente, refletida no relato de patologia do tumor e relata a agressividade do tumor. O prognóstico associado ao CCR Sarcomatoide geralmente é desfavorável. A condição é frequentemente encontrada em pacientes cujo câncer renal realizou metástase de forma ampla. Esta forma de câncer renal é, alguma vezes, tratada com quimioterapia.
-Carcinoma de Células Transicionais do Rim (CCT)
Carcinoma de células transicionais (CCT) do rim é um tumor raro e potencialmente muito agressivo que não deve ser considerado um verdadeiro câncer renal, mas ao invés, deve ser agrupado com aqueles cânceres que se desenvolvem a partir da linha do trato urinário. Isto inclui CCT da bexiga, que é muito mais comum do que CCT do rim. Se o câncer não se espalhou, o tumor pode ser tratado por remoção cirúrgica tanto do rim quanto do ureter, embora recorrências de CCT na bexiga sejam comuns. Quando o tumor é grande ou ocorreu metástase, o prognóstico é extremamente desfavorável e as opções de tratamento são semelhantes àquelas para câncer de bexiga metastático, que inclui quimioterapia.
SUBTIPOS
Oncocitoma Renal
Este é um tumor benigno do rim que soma aproximadamente 5% de todos os tumores de rim. Não ocorre metástase destes tumores, embora possam crescer a tal tamanho no rim e invadir estruturas locais, que podem resultar em sintomas que requerem cirurgia. Eles são considerados relacionados ao CCR cromófobo e pode ser muito difícil diferenciar os dois. O tumor é tratado através de remoção parcial ou completa do rim.
A escolha do tratamento, onde o tratamento é feito, a frequência de check-ups e muitos outros aspectos do controle da doença são determinados pelo paciente e o médico. Alguns pacientes acreditam que as informações sobre o câncer renal são apresentadas em termos médicos complicados. Mas, muitas informações, incluindo os recursos recomendados neste guia são especificamente escritos para pacientes em uma linguagem fácil de entender a qual não requer treinamento especializado.
Quanto mais você souber, melhores serão suas decisões, e mais você se sentirá no controle da sua doença. O conhecimento sobre a sua doença o ajudará a se comunicar melhor com seu médico e enfermeira e aumentará sua confiança no tratamento que você recebe. Saber mais sobre o câncer renal é um passo importante para lutar efetivamente contra a doença.
- Fatores de Risco
-
Como prevenir?
NÃO FUMAR → O tabagismo aumenta significativamente o risco do câncer renal. O risco aumentado parece estar relacionado a quantidade que você fuma. O risco cai se você parar de fumar, mas leva muitos anos para se aproximar ao nível de alguém que nunca fumou;
SOBREPESO/OBESIDADE → Manter uma alimentação saúdavel. Abuse de frutas, verduras e legumes. Elas são as maiores fontes de micronutrientes e ajudam na regulação do organismo. As pessoas que estão muito acima do peso apresentam um risco mais alto de desenvolvimento de câncer de células renais. Alguns médicos acreditam que a obesidade é um fator em certa de 2 de 10 pessoas que adquirem este câncer. A obesidade pode provocar alterações em determinados hormônios que podem levar ao carcinoma de células renais;
PRATIQUE EXERCÍCIO FÍSICO → O sobrepeso e a obesidade podem provocar alterações hormonais que levam ao desenvolvimento do câncer;
MODERE NO SAL E REDUZA O AÇÚCAR → evitando a retenção de liquído, alta pressão arterial e diabetes;
BEBA ÁGUA → ela hidrata o organismo e mantém o bom funcionamento dos rins!
Fatores de Risco
Um fator de risco é qualquer coisa que afete suas chances de contrair uma doença, como um câncer. Diferentes tipos de cânceres apresentam diferentes fatores de risco. Por exemplo, a exposição sem proteção a fortes raios solares é um fator de risco para câncer de pele. Mas os fatores de risco não nos dizem tudo. Apresentar um fator de risco, ou mesmo vários fatores de risco, não significa que você terá a doença. E algumas pessoas que adquirem a doença podem não ter apresentado nenhum dos fatores de risco conhecidos. Mesmo se a pessoa com câncer renal apresentar um fator de risco, em geral é muito difícil saber o quanto aquele fator de risco pode ter contribuído para o câncer.
Fatores de risco Genéticos e Hereditários:
Algumas pessoas herdam uma tendência de desenvolver determinados tipos de câncer. O DNA que você herda dos seus pais pode conter determinadas alterações que contribuem para esta tendência de desenvolver câncer. O câncer renal pode ser causado por algumas condições raras herdadas. Pessoas com estas condições apresentam um risco muito mais alto de adquirir câncer renal, embora elas contribuam apenas para uma pequena parte dos casos no total.
Entre os fatores de risco Genéticos e Hereditários estão:
Carcinoma de Células Renais Papilar Hereditário
Pessoas com esta condição apresentam uma tendência herdada de desenvolver um ou mais carcinomas de células renais papilares, porém eles não apresentam tumores em outras partes do corpo, como é o caso de outras condições herdadas listadas aqui. Pensa-se que este distúrbio seja causado por alterações no gene MET.
Doença von Hippel-Lindau
Pessoas com esta condição frequentemente desenvolvem vários tipos de tumores e cistos (bolsas preenchidas por fluídos) em diferentes partes do corpo. Eles apresentam risco aumentado de desenvolver carcinoma de células renais de células claras, especialmente quando mais jovens. Eles também podem apresentar tumores benignos nos olhos, cérebro, medula espinhal, pâncreas e outros órgãos; e um tipo de tumor da glândula suprarrenal chamado feocromocitoma. Esta condição é provocada por mutações (alterações) no gene VHL.
Leiomiomatose Hereditária e Carcinoma de Células Renais
Pessoas com esta síndrome desenvolvem tumores de músculo liso chamados leiomiomas ou fibroides da pele e do útero (em mulheres) e apresentam um risco mais alto de desenvolver cânceres de células renais papilares. Está ligado a alterações no gene da fumarato hidratase (FH).
Síndrome Birt-Hogg-Dube
Pessoas com esta síndrome, que é caracterizada pelo desenvolvimento de pequenos tumores cutâneos benignos, apresentam um risco aumentado de desenvolver diferentes tipos de cânceres de células renais. Eles também podem apresentar tumores benignos ou malignos de vários outros tecidos. O gene ligado a esta condição é conhecido como BHD.
Oncocitoma Renal Hereditário
Algumas pessoas herdam a tendência de desenvolver um tumor de rim chamado oncocitoma, que apresenta um potencial muito baixo de ser maligno. É importante que as pessoas que apresentam causas hereditárias de câncer de células renais visitem seus médicos com frequência, particularmente se elas já têm câncer de células renais diagnosticadas. Alguns médicos recomendam testes de imagem regulares (como exames de CT) para estas pessoas.
Outros
Há alguns fatores de risco que não podem ser alterados, mas podemos aprender a observá-los e relatar qualquer alteração à equipe médica. São eles:
Histórico Familiar de Câncer Renal
As pessoas com um forte histórico familiar de câncer de células renais (sem uma das condições herdadas conhecida listada acima) também apresentam alta chance de desenvolvimento deste câncer. Este risco é ainda mais alto em irmãos (irmãos ou irmãs) daqueles afetados. Se não está claro se é devido à genética, uma exposição ambiental compartilhada, ou alguma combinação destes.
Alta Pressão Arterial
O risco de câncer renal é mais alto em pessoas com alta pressão arterial. Alguns estudos sugeriram que determinados medicamentos utilizados para tratar alta pressão arterial pode desenvolver o risco de câncer renal, mas é difícil dizer se a condição ou a medicação (ou ambos) podem ser a causa do risco aumentado.
Determinados Medicamentos
Fenacetina, um remédio popular para alívio de dor com venda livre, esteve ligado ao câncer de células renais no passado. Alguns estudos sugeriram que diuréticos (medicamentos que tratam a alta pressão arterial provocando que os rins removam o sal e fluído do corpo) podem estar ligados ao carcinoma de células renais. Não está claro se a causa é dos medicamentos ou da alta pressão arterial em si. Se você precisa de diuréticos, você deve tomá-los. Se não precisa, evite-os para tentar reduzir o risco de câncer renal.
Doença de Rim Avançada
Pessoas com doença de rim avançada, especialmente aqueles que precisam de diálise, apresentam um risco mais alto de carcinoma de células renais. A diálise é um tratamento utilizado para remover toxinas do seu corpo caso os rins não funcionem apropriadamente.
Gênero
O carcinoma de células renais e quase duas vezes tão comum em homens quanto em mulheres. Os homens estão provavelmente mais propensos a fumar e a estarem expostos a elementos químicos que provocam câncer no trabalho, que podem contribuir com uma parte da diferença.
Raça
Negros apresentam uma taxa ligeiramente mais alta de câncer de células renais do que brancos. As razões para isto não estão claras.
Sabemos o que causa o câncer renal?
Embora muitos fatores de risco possam elevar sua chance de desenvolver câncer renal, não se sabe ainda de forma exata como alguns desses fatores de risco tornam as células do rim cancerígenas.
Alterações Genéticas
Pesquisadores estão começando a entender como algumas alterações no DNA podem resultar na modificação de células do rim normais em células cancerígenas.
DNA é a molécula química em cada uma de nossas células que compõe nossos genes – as instruções sobre como nossas células funcionam.
Nós geralmente parecemos com os nossos pais porque eles são a fonte de nosso DNA . Contudo, o DNA afeta mais do que nossa aparência.
Alguns genes contêm instruções para controle de quando nossas células devem crescer, se dividir e morrer. Determinados genes que aceleram a divisão celular são chamados oncogenes. Outros genes que diminuem a velocidade da divisão celular ou fazem com que as células morram no momento certo são denominados genes supressores de tumor.
O câncer pode ser causado por mutações do DNA (alterações) que ativam os oncogenes ou desativam os genes supressores de tumor.
Mutações Genéticas Herdadas
Determinadas alterações do DNA herdadas podem levar a condições correntes em algumas famílias que aumentam o risco de câncer renal.
Estas síndromes, que provocam uma pequena parte de todos os cânceres renais, foram descritas na seção Fatores de Risco.
Por exemplo, o gene VHL é um gene supressor de tumor. Ele normalmente ajuda a impedir que as células cresçam fora de controle. As mutações (alterações) neste gene podem ser herdada de um dos pais, provocando a doença von Hippel-Lindau. Quando ocorre mutação no gene VHL, ele não mais suprime o crescimento anormal e é mais provável que o câncer renal se desenvolva.
Os genes ligados à leiomiomatose hereditária, ao carcinoma de células renais (o gene da fumarato hidratase) e à síndrome Birt-Hogg-Dube (o gene BHD) também são genes supressores de tumor, e as alterações herdadas nestes genes também levam a um risco aumentado de câncer renal.
Pessoas com carcinoma de células renais papilar hereditário herdam alterações no oncogene MET que podem provocar que fique “ativo” o tempo todo. Isto torna a pessoa mais propensa a desenvolver câncer de células renais papilar.
Mutações Genéticas Adquiridas
A maioria das mutações de DNA relacionadas ao câncer de mama, entretanto, ocorre durante a vida da pessoa ao invés de ser herdada. Estas mutações adquiridas de oncogenes e/ou dos genes supressores de tumor podem resultar de fatores como exposição a elementos químicos que provocam câncer (como aqueles encontrados no tabaco), porém em muitos casos a causa destas alterações não é conhecida.
Cerca de 3 de 4 pessoas com câncer de células renais claras esporádico (não-herdado) apresentam alterações no gene VHL que provoca que este não funcione apropriadamente. Estas alterações foram adquiridas durante a vida ao invés de serem herdadas.
Outras alterações genéticas também podem provocar carcinomas de células renais. Os pesquisadores continuam a procurar estas alterações.
Algum progresso foi alcançado na compreensão em como o tabaco aumenta o risco de desenvolvimento de carcinoma de células renais. Muitos dos elementos que provocam câncer no tabaco são absorvidos pela corrente sanguínea pelos pulmões. Como os rins filtram este sangue, muitos destes elementos tornam-se altamente concentrados nos rins.
Vários destes elementos químicos são conhecidos por danificar o DNA das células renais de forma que pode tornar células normais em cancerígenas.
A obesidade, outra causa deste câncer, altera o equilíbrio de alguns dos hormônios do corpo. Os pesquisadores estão agora aprendendo como determinados hormônios ajudam a controlar o crescimento (tanto normal quanto anormal) de muitos tecidos diferentes no corpo, incluindo os rins.
Conhecimento das alterações genéticas que podem levar ao câncer de mama está sendo utilizado para ajudar a desenvolver novos tratamentos para esta doença. Por exemplo, os pesquisadores agora sabem que o gene VHL normalmente impede que as células produzam uma substância chamada fator do crescimento endotelial vascular (VEGF). Esta substância provoca a formação de novos vasos sanguíneos, dos quais os tumores precisam para sobreviver e crescer. Medicamentos recentes que têm como alvo o VEGF estão agora sendo utilizados para tratar o câncer renal.
- Sintomas
-
Alguns possíveis sinais e sintomas de câncer renal incluem:
> sangue na urina (hematúria);
> dor lombar em um lado (não provocada por lesão);
> uma massa ou inchaço no lado ou na região lombar;
> fadiga;
> perda de peso não explicada;
> febre que não é causada por um resfriado ou outra infecção e que não passa após poucas semanas;
> inchaço dos tornozelos e pernas (edema);
Estes sintomas podem ser causados pelo câncer, mas com mais frequência se dão devido a doenças não-cancerosas. Por exemplo, sangue na urina pode ser um sinal de câncer renal, bexiga ou de próstata, mas com muita frequência é provocado por infecção na bexiga ou pedra no rim. Ainda, se você apresentar algum destes sintomas, consulte um médico, assim a causa pode ser avaliada e tratada, se necessário.
- Diagnóstico
-
Como o Câncer Renal é Diagnosticado?
Muitos cânceres renais são encontrados regularmente de forma precoce, enquanto eles ainda estão confinados no rim. Porém, outros são encontrados em um estágio mais avançado. Há algumas razões para isto:
> Estes cânceres podem, algumas vezes, se tornar muito grandes sem provocar nenhuma dor ou outros problemas;
> Devido ao fato do rim estar muito adentro do corpo, pequenos tumores do rim não podem ser observados ou sentidos durante um exame físico;
> Não há testes simples que possam ser utilizados para examinar o câncer renal em pessoas que não estão em risco aumentado.
Um teste de urina de rotina, que, às vezes, é parte de um exame médico completo, pode encontrar pequenas quantidades de sangue na urina de algumas pessoas com câncer de células renais precoce. Porém, há muitas outras causas de sangue na urina, incluindo infecções do trato urinário, infecções da bexiga, câncer da bexiga e condições benignas do rim (não cancerosas), tais como pedras no rim.
Por outro lado, algumas pessoas com câncer renal não apresentam sangue na urina até que o câncer esteja muito grande e possa ter se espalhado para outras partes do corpo. Exames de imagem, tais como exames de tomografia computadorizada (CT) e exames de imagem por ressonância magnética (MRI) podem encontrar pequenos carcinomas de células renais. Mas estes exames são caros e nem sempre revelam tumores benignos de pequenos carcinomas de células renais. Por estas razões, os médicos geralmente recomendam CT e MRI para detecção precoce de câncer renal apenas em pessoas que apresentam determinados fatores de risco, tais como doença von Hippel-Lindau (VHL) ou outras condições herdadas. Alguns médicos também recomendam que pessoas com doenças de rim tratadas por diálise em longo prazo realizem testes periódicos (exames de CT ou MRI) para procurar por câncer renal. Em geral, cânceres renais são encontrados incidentalmente durante exames para algumas outras doenças, tais como doença de vesícula biliar. Estes cânceres geralmente não provocam dor ou desconforto no momento da descoberta. A taxa de sobrevida para câncer renal descoberto desta forma é muito alta, pois estes cânceres geralmente são descobertos em um estágio muito precoce.Saiba mais sobre diagnóstico precoce:
É importante dizer ao seu médico se familiares (parentes de sangue) apresentam ou apresentaram câncer renal, especialmente quando jovens, ou se eles foram diagnosticados com uma condição herdada ligada a este câncer, como doença VHL. Seu médico pode recomendar que você considere o teste genético. O teste genético para estas condições é utilizado apenas em pessoas com sinais clínicos destas condições e em seus parentes de sangue. Antes de realizar os testes genéticos, é importante falar com um consultor genético, assim você entende o que os testes podem – e não podem – dizer a você, e o que alguns resultados significariam. Os testes genéticos procuram mutações genéticas que provocam estas condições no seu DNA. Eles são utilizados para diagnosticar estas condições herdadas, não o câncer renal em si. Seu risco pode estar aumentado se você apresentar uma destas condições, mas isto não significa que você apresenta (ou definitivamente apresentará) câncer renal. Se você foi diagnosticado com uma destas condições, você pode precisar de frequentes exames de CT ou MRI para procurar por câncer renal.
Para o dignóstico do câncer renal são utilizados exames de imagem e laboratóriais. Abaixo listados os exames necessários para diagnosticar o câncer renal:
Exames de Imagem
Exames por imagem utilizam raios-X, campos magnéticos ou substâncias radioativas para criar fotos de dentro do seu corpo. Exames de imagem podem ser realizados por um número de motivos, incluindo ajudar a descobrir se a área suspeita pode ser cancerosa, saber o quão longe o câncer pode ter se espalhado e ajudar a determinar se o tratamento foi eficaz. Diferente da maioria dos outros cânceres, os médicos podem com frequência ter certeza sobre o diagnóstico do câncer renal sem precisar realizar uma biópsia (remoção de uma amostra do tumor para ser observado em microscópio). Em muitos casos, os exames de imagem podem dar aos médicos uma quantidade razoável de certeza que uma massa do rim é (ou não) cancerosa. Em alguns casos, no entanto, uma biópsia pode ser necessária para ter certeza. Exames de tomografia computadorizada (CT), exames de imagem por ressonância magnética (MRI), pielogramas intravenosos e ultrassom podem ser muito úteis no diagnóstico na maioria dos tipos de tumores renais, embora os pacientes raramente precisem de todos estes exames. Outros exames descritos aqui, como raios-X do tórax e exames ósseos são utilizados com mais frequência para ajudar a determinar se o câncer se propagou (ocorreu metástase) para outras partes do corpo.
Exame de Tomografia Computadorizada (CT ou CAT)
O exame de Exame de Tomografia Computadorizada (CT ou CAT) consiste em um exame de raio-X que produz imagens seccionais cruzadas detalhadas do seu corpo. Ao invés de tirar uma fotografia, como um raio-X convencional, o aparelho de CT obtém diversas imagens conforme gira ao seu redor, enquanto você está deitado em uma mesa. Então, um computador combina essas imagens na forma de imagens de fatias da parte do corpo que está sendo estudada. Diferente de um raio-X convencional, um exame de CT cria imagens detalhadas dos tecidos moles no corpo. Depois de obtido o primeiro grupo de imagens, pode ser solicitado que você beba uma solução de contraste e/ou você pode receber um cateter IV (intravenoso) por meio do qual é injetado um corante de contraste. Ele ajuda a delinear melhor as estruturas do seu corpo. Em seguida, se obtém um segundo grupo de imagens.
O contraste pode provocar um pouco de rubor (uma sensação de calor, especialmente na face). Algumas pessoas são alérgicas e apresentam urticária. Raramente, podem ocorrer reações mais sérias como dificuldades para respirar ou queda da pressão arterial. Não deixe de informar o médico caso você sofra ou já tenha sofrido alguma reação a qualquer material de contraste utilizado para raios-X.
Exames de CT são mais demorados do que raios-X convencionais. Você precisa ficar deitado em uma mesa durante sua realização. Durante o exame, a mesa se movimenta para dentro e para fora do aparelho, uma máquina em formato de anel que envolve completamente a mesa. Você pode se sentir um pouco confinado pelo anel em que deve se deitar enquanto as imagens são obtidas.
Nos últimos anos, a CT espiral (também conhecida como CT helicoidal) se tornou disponível em muitos centros médicos. Este tipo de exame de CT utiliza uma máquina mais rápida. A parte da máquina que obtém a imagem roda em volta do corpo continuadamente, permitindo que os médicos coletem as imagens mais rapidamente do que com a CT padrão. Isto reduz a chance de imagens “borradas” decorrentes do movimento de respiração. Também diminui a dose de radiação recebida durante o exame. A maior vantagem pode ser que as “fatias” de imagem que ele obtém são mais finas, o que proporciona imagens mais detalhadas e permite que médicos olhem as áreas suspeitas de diferentes ângulos.
O exame de CT é um dos exames mais úteis para achar e olhar uma massa dentro do rim. Ele também é útil para verificar se um câncer se espalhou, ou não, para órgãos e tecidos além do rim. O exame de CT fornecerá informações precisas sobre o tamanho, formato e posição de um tumor, e pode ajudar a encontrar linfonodos maiores que possam conter câncer.
Imagem por Ressonância Magnética (MRI)
Assim como os exames de Tomografia Computadorizada (CT), os exames de Imagem por Ressonância Magnética (MRI) fornecem imagens detalhadas de tecidos moles no corpo.
Exames de MRI são utilizados com menos frequência do que os exames de CT em pessoas com câncer renal. Eles podem ser realizados em casos onde os exames de CT não são práticos, tais como se a pessoa for alérgica ao contraste de CT.
Exames de MRI também podem ser realizados se houver uma chance do câncer envolver uma veia principal no abdômen (veia cava inferior). Finalmente, eles podem ser utilizados para procurar possível propagação do câncer para o cérebro ou para a medula espinhal se uma pessoa apresentar sintomas que sugerem que este possa ser o caso.
Ultrassom (ultrassonografia ou US)
O ultrassom utiliza ondas sonoras para criar imagens de órgãos internos.
Para este exame, um pequeno instrumento semelhante a um microfone chamado transdutor é colocado na pele próximo ao rim. Ele emite ondas sonoras e capta os ecos conforme eles são refletidos pelos tecidos no rim. Os ecos são convertidos por um computador em uma imagem em preto e branco que é exibida em uma tela de computador. Este exame é indolor e não expõe você à radiação.O ultrassom pode ser útil para determinar se uma massa do rim é sólida ou preenchida por fluído. Os modelos de eco produzidos pela maioria dos tumores do rim parecem diferentes daqueles do tecido do rim normal.
Diferentes modelos de eco também podem distinguir alguns tipos de tumores benignos e malignos do rim um do outro. Se uma biópsia de rim for necessária, este exame pode ser utilizado para guiar uma agulha da biópsia na massa para obter uma amostra.
Exame de Tomografia por Emissão de Pósitron (PET SCAN)
Exames de PET SCAN envolvem a injeção de uma forma de açúcar radioativo (conhecido como fluorodeoxiglicose ou FDG) no sangue. A quantidade de radioatividade utilizada é muito baixa.
Como as células cancerosas do corpo crescem rapidamente, elas absorvem grandes quantidades do açúcar radioativo. Uma câmera especial pode, assim, gerar uma imagem de áreas de radioatividade do corpo. A imagem não é extremamente detalhada como um exame de CT ou MRI, mas proporciona informações úteis sobre o corpo todo.
Este exame pode ser útil para observar se o câncer pode ter se espalhado para os linfonodos próximos ao rim. Exames de PET também podem ser úteis quando o médico acredita que o câncer possa ter se espalhado, mas não tem conhecimento de onde isso ocorreu. Exames de PET podem ser utilizados ao invés de diversos raios-X diferentes, pois eles realizam varredura do corpo inteiro.
Algumas máquinas mais recentes conseguem realizar tanto um exame de PET quanto um exame de CT ao mesmo tempo (exame PET/CT). Isso permite ao radiologista comparar áreas de maior radioatividade no PET com a aparência da mesma área na CT.
Pielograma Intravenoso (IVP)
Um pielograma intravenoso é um raio-X do sistema urinário realizado após um corante especial ter sido injetado na veia. Este corante sai da corrente sanguínea para os rins e, então, passa pelos ureteres e bexiga.
Um IVP pode ser útil para encontrar anormalidades do trato urinário, tais como câncer, mas você pode não precisar de um IVP caso já tenha realizado uma CT ou MRI.
Angiografia
Assim como IVP, este exame de raio-X também utiliza um corante de contraste. Um cateter é geralmente preso a uma artéria de grande porte na sua perna na artéria que segue para o rim (artéria renal). O corante é, então, injetado na artéria para contornar os vasos sanguíneos.
Como a angiografia pode contornar os vasos sanguíneos que alimentam o tumor do rim, ela pode ajudar o cirurgião a planejar uma cirurgia. A angiografia também pode ajudar a diagnosticar cânceres renais uma vez que os vasos sanguíneos geralmente apresentam uma aparência especial com este exame.
Raio-X do Tórax
Se o câncer renal foi diagnosticado (ou há suspeita), um raio-X plano do seu tórax pode ser realizado para observar se o câncer se propagou para os pulmões. Isto é muito improvável, a menos que o câncer esteja muito avançado. Este raio-X pode ser realizado em qualquer contexto ambulatorial. Se os resultados forem normais, provavelmente você não apresenta câncer nos pulmões.
Exame Ósseo
Um exame ósseo pode ajudar a mostrar se o câncer sofreu metástase (se espalhou) para os ossos. Nesse exame, é injetada uma pequena quantidade de material de baixo nível de radioatividade em uma veia (por via intravenosa, ou IV). A substância se deposita nas áreas do osso comprometido por todo o esqueleto, no decorrer de algumas horas. Então, você fica deitado sobre uma mesa por cerca de 30 minutos enquanto uma câmera especial detecta a radioatividade e gera uma imagem do seu esqueleto.
Áreas de alterações ósseas ativas como “hot spots” no seu esqueleto – ou seja, elas atraem a radioatividade. Essas áreas podem sugerir a presença de câncer metastático, no entanto, a artrite e outras doenças ósseas também podem produzir o mesmo padrão. Para distinguir entre essas condições, sua equipe de cuidados oncológicos pode utilizar outros exames de imagem, como raios-x simples ou exames de CT e MRI, para conseguir uma visualização melhor das áreas realçadas, ou podem até mesmo colher amostras do osso para biópsia.
Exames ósseos são realizados principalmente quando há motivo para pensar que o câncer possa ter se espalhado para os ossos (pois uma pessoa apresenta sintomas como dor óssea). Exames de PET geralmente também podem mostrar a propagação do câncer para os ossos, portanto, se você realizou um exame de PET você pode não precisar de um exame ósseo.
Exames Laboratoriais
Exames laboratoriais geralmente não são utilizados para diagnosticar câncer renal, mas eles podem, algumas vezes, dar a primeira pista de que pode haver um problema com os rins. Eles também são realizados para ter uma ideia da saúde geral da pessoa e para ajudar a dizer se o câncer pode ter se espalhado para outras áreas. Antes da cirurgia, eles podem ajudar a dizer se uma pessoa é saudável o suficiente para realizar a operação.
Exame de Urina (Urinálise)
O Exame de Urina (Urinálise) é, algumas vezes, parte de um exame físico completo, mas ele pode não ser realizado como parte de exames físicos de rotina. É provável que seja um dos primeiros exames realizados caso o câncer renal seja uma possibilidade.
Exames microscópicos e químicos são realizados na urina para procurar pequenas quantidades de sangue e outras substâncias não observadas a olho nu. Cerca de metade dos pacientes com câncer de células renais apresentam sangue na urina. Algumas vezes, exame microscópico especial de amostras da urina (chamado citologia da urina) mostrará células cancerosas reais na urina.
Hemograma
O hemograma pode detectar achados algumas vezes observados com câncer de células renais. Anemia (pouquíssimos eritrócitos) é muito comum. Com menos frequência, uma pessoa pode apresentar muitos eritrócitos, pois o câncer renal produz um hormônio (eritropoietina) que provoca que a medula óssea produza mais eritrócitos. As contagens de sangue também são importantes para se certificar que uma pessoa é saudável o suficiente para uma cirurgia.
Exames de Bioquímica do Sangue
Exames de bioquímica do sangue geralmente são realizados em pessoas que possam apresentar câncer renal, uma vez que ele pode afetar os níveis de determinados elementos químicos no sangue. Por exemplo, altos níveis de enzimas hepáticas são encontrados algumas vezes, embora os motivos para isso não sejam conhecidos. Altos níveis de cálcio no sangue podem indicar que o câncer se espalhou para os ossos e pode, portanto, alertar o médico para solicitar um exame ósseo.
Biópsia por Aspiração com Agulha Fina
Este exame é raramente utilizado para diagnosticar tumores de rim. Estudos por imagem geralmente fornecem informações suficientes para um cirurgião decidir se a operação é ou não necessária. Algumas vezes a biópsia por aspiração com agulha fina (FNA) é utilizada para obter pequena amostra das células de uma área suspeita se os resultados do exame de imagem não forem conclusivos o suficiente para garantir a remoção do rim. Ela também pode ser realizada para confirmar o diagnóstico de câncer se a saúde da pessoal for muito deficiente para cirurgia e outros tratamentos locais (tais como embolização arterial ou crioterapia) estão sendo considerados. Para este exame, a pele onde a agulha será inserida é, em primeiro lugar, adormecida com anestesia local. O médico direciona uma agulha vazia na área enquanto observa seu rim com exames de ultrassom ou CT. Diferente do ultrassom, a CT não fornece uma imagem contínua, então a agulha é inserida na direção da massa, uma imagem de CT é obtida e a direção da agulha é orientada com base na imagem. Isto é repetido algumas vezes até a agulha estar dentro da massa. Uma pequena amostra da área-alvo é sugada (aspirada) para uma seringa e observada em microscópio para observar se células cancerosas estão presentes. Em casos onde os médicos pensam que o câncer renal possa ter se espalhado para outros locais, eles podem realizar uma biópsia do local metastático ao invés do rim.
Grau de Fuhrman
O grau de Fuhrman é determinado pela observação das células do câncer renal (obtidas durante uma biópsia ou durante cirurgia) em um microscópio. Ele é utilizado por muitos médicos como uma maneira de descrever o quão agressivo o câncer provavelmente pode ser. O grau é baseado em o quanto os núcleos das células cancerosas (parte de uma célula na qual o DNA é armazenado) se parece com aqueles de células de um rim normal. Os cânceres de células renais geralmente são graduados em uma escala de 1 até 4. Os cânceres de células renais grau 1 têm núcleos celulares que diferem muito pouco dos núcleos celulares de um rim normal. Estes cânceres normalmente crescem e se espalham lentamente e tendem a apresentar uma boa perspectiva. No outro extremo, núcleos de câncer de células renais grau 4 são muito diferentes de núcleos de células de um rim normal e apresentam um pior prognóstico. Embora o tipo celular e o grau algumas vezes sejam úteis na previsão do prognóstico, o estágio do câncer está longe de ser a melhor previsão de sobrevida. O estágio descreve o tamanho do câncer e o quanto ele se espalhou além do rim.
- Tratamento
-
Como é tratado?
O tratamento varia de pessoa para pessoa. A escolha depende muito do estágio do câncer, do estilo de vida do paciente e da alimentação. Após a determinação do câncer e de seu estágio, a equipe de cuidados oncológicos discutirá com o paciente as opções de tratamento. No caso do câncer renal, as opções de tratamento podem incluir cirurgia, terapia por radiação, terapia-alvo, imunoterapia, quimioterapia ou outras dessas combinações, dependendo dos fatores acima mencionados.
Tipos de Tratamento
Cirurgia
A cirurgia é o principal tratamento para a maioria dos carcinomas de células renais. As chances de sobreviver a um câncer de célula renal sem cirurgia são pequenas. Dependendo do estágio e do local do câncer e outros fatores, a cirurgia pode ser usada para remover tanto o câncer com alguns tecidos circundantes do rim quanto o rim em sua totalidade.
Radioterapia
A Radioterapia usa radiação de alta energia para matar as células cancerígenas. A terapia por feixe externo foca a radiação a partir do lado de fora do corpo sob o câncer. É como fazer um raio-x, mas a radiação é muito mais intensa. O procedimento em si é indolor. A radioterapia pode ser usada para tratar o câncer renal se a saúde geral da pessoa estiver muito debilitada para passar por cirurgia. Infelizmente, os cânceres renais não são muito sensíveis à radiação. Usar radioterapia antes ou após a remoção do câncer, não é rotineiramente recomendado porque os estudos não mostraram que ela melhora as taxa de sobrevida.
Quimioterapia
Quimioterapia usa medicamentos anticâncer que são administrados na veia ou pela boca (em forma de pílulas). Esses medicamentos entram na corrente sanguínea e alcançam todas as áreas do corpo, o que torna o tratamento potencialmente útil para o câncer que se disseminou (metastatizado) para os órgãos além dos rins.Infelizmente, as células do câncer renal são geralmente resistentes à quimioterapia, e não existe nenhuma maneira padrão de tratá-las com esses medicamentos. A quimioterapia é geralmente reservada para cânceres onde os medicamentos alvo e/ou imunoterapia não são eficazes.
Terapia-alvo
A terapia alvo é considerada uma medida terapêutica que veio revolucionar o tratamento do câncer, causando menos danos às células sadias. Utilizam anticorpos monoclonais, capazes de limitar o crescimento do tumor, em uma ação semelhante ao nosso sistema imunológico. Cerca de 20 a 25% dos casos se beneficiam dessa alternativa.
Imunoterapia
Segundo o Instituto Nacional do Câncer – INCA, é chamado de imunoterapia o tratamento do câncer que promove a estimulação do sistema imunológico, por meio do uso de substâncias modificadoras da resposta biológica. A imunoterapia é classificada em ativa e passiva, de acordo com as substâncias utilizadas e os seus mecanismos de ação. Na imunoterapia ativa, substâncias estimulantes e restauradoras da função imunológica (imunoterapia inespecífica) e as vacinas de células tumorais (imunoterapia específica) são administradas com a finalidade de intensificar a resistência ao crescimento tumoral. Na imunoterapia passiva ou adotiva, anticorpos antitumorais ou células mononucleares exógenas são administradas, objetivando proporcionar capacidade imunológica de combate a doença.
Curiosidades sobre o câncer renal:
- Você sabe a quantidade ideal que você deve consumir de água por dia? Saiba que cada pessoa possui uma quantidade ideal. Descubra qual a sua no site do Instituto Espaço de Vida e comece agora a beber a sua quantidade ideal!
- Voce sabe quanto pesa o seu rim? 150 gramas é o peso de cada um dos seus rins.
- Os cálculos Renais aumentam cerca de 30% durante o verão. Por isso, fique atento!
- Estadiamento
-
Como o Câncer Renal é Classificado?
O estadiamento é o processo de descobrir o quanto o câncer se espalhou. Seu tratamento e prognóstico (a previsão de chances de sobrevida) dependem, em grande parte, do estágio do câncer.
O estadiamento está baseado em resultados de exame físico, biópsias e exames de imagem (exame de CT, raio-X do tórax, exame de PET, etc.).
Na verdade, há 2 tipos de estadiamento para o câncer renal. O estágio clínico é a melhor estimativa do seu médico da extensão da sua doença, com base nos resultados de exame físico, exames laboratoriais e qualquer estudo de imagem que você tenha realizado. Se você realizar cirurgia, seus médicos também podem determinar o estágio patológico, que é baseado em alguns fatores como estágio clínico, mais o que for encontrado durante a cirurgia e exame do tecido removido. Isto significa que se você realizar uma cirurgia, o estágio do câncer pode realmente mudar depois disso (se foi descoberto que o câncer se espalhou mais do que estava suspeito, por exemplo). Provavelmente, o estadiamento patológico é mais preciso que o clínico, já que permite ao médico obter uma impressão direta da extensão do câncer.
Sistema de Estadiamento AJCC (TNM)
O sistema de estadiamento é uma maneira padronizada no qual a equipe de tratamento oncológico descreve a extensão do câncer. O sistema de estadiamento mais comumente utilizado é o da American Joint Committee on Cancer (Comitê da Junta Americana do Câncer) (AJCC), algumas vezes também conhecido como sistema TNM. O sistema TNM descreve 3 informações-chave:
> T indica o tamanho do tumor principal (primário) e se ele cresceu para as áreas próximas.
> N descreve a extensão de propagação para os linfonodos próximos (regionais). Os linfonodos são pequenos grupos de células do sistema imune em formato de feijão que são importantes na luta contra infecções.
> M indica se o câncer se espalhou (sofreu metástase) para outros órgãos do corpo. (Os locais mais comuns de propagação são para os pulmões, ossos, fígado e linfonodos distantes).
Números ou letras aparecem após T, N e M para fornecer mais detalhes sobre cada um destes fatores. Os números 0 a 4 indicam gravidade crescente. A letra X significa “não pôde ser avaliado, pois as informações não estavam disponíveis”.
Categorias T para Câncer Renal
TX: O tumor primário não pode ser avaliado (informações não disponíveis).
T0: Nenhuma evidência de tumor primário.
T1a: O tumor mede 4 cm (cerca de 11/2 polegadas) em sua extremidade ou é menor e está limitado ao rim.
T1b: O tumor mede mais que 4 cm, mas não maior que 7 cm (cerca de 2 ¾ polegadas) em sua extremidade e ainda está limitado ao rim.
T2: O tumor mede mais que 7 cm em sua extremidade mas ainda é limitado ao rim.
T3a: O tumor se espalhou pela glândula suprarrenal (que está situada sobre o rim) ou dentro do tecido adiposo ao redor do rim, mas não para além da camada fibrosa que circunda o rim e as proximidades do tecido adiposo (Fáscia de Gerota).
T3b: O tumor se espalhou para dentro da veia principal que leva para fora do rim (veia renal) e/ou a parte da maior veia que leva para o coração (veia cava) que está dentro do abdome.
T3c: O tumor atingiu a parte da veia cava que está dentro do tórax ou invadiu a parede da veia cava.
T4: O tumor se espalhou para além da fáscia de Gerota (camada fibrosa ao redor do rim e próximo do tecido adiposo).
Categorias N para Câncer Renal
NX: Os linfonodos regionais (proximidades) não podem ser avaliados (informação não disponível).
N0: Não se espalhou nos arredores dos linfonodos.
N1: Espalhou-se para os arredores de 1 linfonodo.
N2: Espalhou-se para os arredores de mais de 1 linfonodo.
Categorias M para Câncer Renal
MX: A presença de metástase distante não pode ser avaliada (informação não disponível).
M0: Não se espalhou para os linfonodos distantes ou outros órgãos.
M1: Presença de metástase distante; inclui a propagação para os linfonodos distantes e/ou para outros órgãos (tais como pulmões, ossos ou cérebro).
Grupamento por Estágio
Uma vez que as categorias T, N e M foram determinadas, esta informação é combinada para determinar o estágio global de I, II, III ou IV. O estágio identifica cânceres que apresentam um prognóstico semelhante, e portanto, são tratados de maneira semelhante. Os pacientes com estágio de menor número tendem a apresentar prognósticos melhores.
Estágio I
T1a-T1b, N0, M0: O Tumor mede 7 cm ou menos e é limitado ao rim. Não há disseminação para os linfonodos ou órgãos distantes.
Estágio II
T2, N0, M0: O tumor mede mais que 7 cm, mas ainda é limitado ao rim. Não há disseminação para os linfonodos ou órgãos distantes.
Estágio III
Diferentes combinações de categorias T e N são incluídas neste estágio.
T3a-T3c, N0, M0: O tumor principal atingiu a glândula suprarrenal, o tecido adiposo ao redor do rim, a veia renal e/ou a veia principal (veia cava) levando do rim ao coração. Ele não se espalhou para além da fáscia de Gerota. Não há disseminação para os linfonodos ou órgãos distantes.
T1a-T3c, N1, M0: O tumor principal pode ser de qualquer tamanho e pode estar fora do rim, mas não se espalhou para além da fáscia de Gerota. O câncer se espalhou para os arredores de 1 linfonodo mas não se espalhou para os linfonodos distantes ou outros órgãos.
Estágio IV
Existem diversas combinações de categorias T, N e M que estão incluídas neste estágio.
T4, N0-N1, M0: O tumor principal invadiu além da fáscia de Gerota. Espalhou-se para os arredores de mais de 1 linfonodo. Não se espalhou para os linfonodos distantes ou outros órgãos.
Qualquer T, N2, M0: O tumor principal pode ter qualquer tamanho e pode estar fora do rim. O câncer se espalhou para os arredores de mais de 1 linfonodo mas não se espalhou para os linfonodos distantes ou outros órgãos.
Qualquer T, Qualquer N, M1: O tumor principal pode ter qualquer tamanho e pode estar fora do rim. Pode ter se espalhado ou não para perto dos linfonodos. Espalhou-se para os linfonodos distantes e/ou outros órgãos.
Outros Sistemas
Embora o sistema de classificação TNM seja útil, alguns médicos têm apontado que existem outros fatores além da extensão do câncer que devem ser considerados na determinação do prognóstico e tratamento.
Universidade da Califórnia em Los Angeles (UCLA) Sistema de Classificação Integrado
Este é um sistema mais complexo porém provavelmente mais preciso. Junto com o estágio do câncer, leva em consideração a saúde global da pessoa e o grau de Fuhrman do tumor para dividir pessoas em grupos de risco baixo, intermediário e alto. Você pode querer perguntar ao seu médico se ele ou ela usa este sistema e como ele pode se aplicar ao seu caso.
Com formato muito parecido com a de uma borboleta, a glândula tireoide é localizada na parte anterior do pescoço, logo abaixo do Pomo de Adão e é responsável pela produção dos hormônios T3 (triiodotironina) e o T4 (tiroxina) que são essenciais porque interferem em vários controles do organismo, como os batimentos cardíacos, a temperatura, o metabolismo (conjunto de mecanismos químicos necessários ao organismo) que pode ficar mais rápido ou lento, e os movimentos intestinais.
Quais são os tipos de câncer de tireoide?
Carcinoma papilifero – é o mais comum. Pode aparecer em pacientes de qualquer idade, mas é mais freqüente entre 30 e 50 anos. Estima-se que uma a cada mil pessoas tem ou já teve este tipo de câncer. A taxa de cura é alta, chegando a quase 100%.
– Carcinoma folicular – Costuma ocorrer em indivíduos com mais de 40 anos. É mais agressivo do que o papilífero. Em dois terços dos casos, não têm tendência à disseminação. Um tipo de carcinoma folicular mais agressivo é o hurthle, que atinge pessoas com mais de 60 anos.
– Carcinoma medular – Afeta as células parafoliculares, responsáveis pela produção da calcitonia, hormônio que contribui na regulação do nível sanguíneo de cálcio. É de difícil tratamento e, usualmente, se apresenta de moderado a muito agressivo.
– Carcinoma anaplásico ou inmedular – Extremamente raro. Contudo, é do tipo mais agressivo e tem o tratamento mais difícil. É responsável por dois terços dos óbitos de câncer da tireóide.
O que causa o câncer de tireoide e quem está em risco?
A causa exata do câncer de tireoide não é conhecida, mas as pessoas com certos fatores de risco são mais vulneráveis que outras à doença.
Esses fatores de risco incluem:
- tratamentos com radiação para a cabeça, pescoço ou tórax, especialmente na infância ou adolescência
- história familiar de câncer de tireoide
- um grande nódulo ou em rápido crescimento
- idade superior a 40 anos
Ter um fator de risco não significa que você terá câncer de tireoide e algumas pessoas desenvolvem a doença não tem nenhum fator de risco. Ainda assim, ter um nódulo de tireoide com qualquer um desses fatores de risco requer avaliação.
Fonte: ACS
O principal sinal é a aparição de um nódulo indolor na tireoide.
Fonte: ACS
O diagnóstico de câncer na tireoide considera os achados no exame clínico de palpação da glândula e a presença de gânglios linfáticos aumentados. Entretanto, como apenas pequeno número de nódulos é palpável, exames de imagem como a ultrassonografia, a cintilografia e a ressonância magnética são recursos úteis para o diagnóstico. O mais importante, porém, é a biopsia de aspiração com agulha fina para identificar a presença ou não de células tumorais malignas.
Fonte: ACS
Em geral, o tratamento do câncer de tireoide é cirúrgico (tireoidectomia total ou parcial) e leva em conta o tipo e a gravidade da doença. Caso as células malignas tenham comprometido os gânglios cervicais, é necessário retirá-los.
Rouquidão e queda de cálcio são complicações da tireoidectomia associadas a lesões de estruturas como os nervos laríngeos e as glândulas paratireoides respectivamente durante a cirurgia.
Depois de quatro a seis semanas da intervenção, o paciente recebe doses terapêuticas de iodo radioativo em ambiente hospitalar para extinguir qualquer tecido remanescente de células tumorais no corpo e evitar metástases. Quando os carcinomas papilíferos e foliculares não respondem a esse tratamento, é possível recorrer à terapêutica antiangiogênica que consiste em bloquear a formação de novos vasos sanguíneos para impedir que as células tumorais recebam nutrientes e oxigênio através da circulação. O passo seguinte é indicar a reposição hormonal com levotiroxina por via oral para substituir os hormônios que deixaram de ser produzidos pela tireoide. Radioterapia, associada ou não à quimioterapia, é recomendada na ocorrência de tumores mais agressivos, como o carcinoma medular e o carcinoma anaplásico.
Fonte: ACS
É preciso que o médico e o paciente estejam sempre atentos ao estadiamento da doença! Mas, o que é estadiamento? São os estágios que o câncer está no momento, ou seja, o tamanho, a localização e se espalhou para outros órgãos. O estádio de um tumor reflete não apenas a taxa de crescimento e a extensão da doença, mas também o tipo de tumor e sua relação com o hospedeiro. O sistema de estadiamento mais utilizado é o TNM da American Joint Committee on Cancer.
O que é TNM?
É a abreviatura de tumor, linfonodo e metástase. Este sistema utiliza três critérios para avaliar o estágio do câncer:
-
O próprio tumor ( T + um número de 0 a 4 usa-se para descrever o tumor primário);
-
Os linfonodos regionais ao redor do tumor ( N + 0 a 3 usa-se para descrever se a doença disseminou para os gânglios linfáticos)
-
E se o tumor se espalhou para outras partes do corpo (M usa-se para descrever que a doença se espalhou para outros órgãos)
O estadiamento pode ser clínico e patológico. O estadiamento clínico é estabelecido a partir dos dados do exame físico e dos exames complementares. O estadiamento patológico baseia-se nos achados cirúrgicos e no exame anátomopatológico – é estabelecido após tratamento cirúrgico e determina a extensão da doença com maior precisão. Lembrando que o estadiamento patológico pode ou não coincidir com o estadiamento clínico e não é aplicável a todos os tumores.
E o estadiamento do câncer da TIREOIDE, como funciona?
Categorias T para o câncer de tiróide (exceto o câncer anaplásico de tireoide)
TX: O tumor primário não pode ser avaliado.
T0: Nenhuma evidência de tumor primário.
T1: O tumor é de 2 cm (um pouco menos de uma polegada) em toda ou menor e não cresceu fora da tireoide.
-
T1a: O tumor tem 1 cm de diâmetro ou menos e não cresceu fora da tireoide.
-
T1b: O tumor é maior do que 1 cm mas não maior do que 2 cm de diâmetro e não cresceu fora da tireoide.
T2: O tumor tem mais de 2 cm de diâmetro, mas não mais de 4 cm e não cresceu fora da tireoide.
T3: O tumor é maior que 4 cm de diâmetro, ou apenas começou a crescer em tecidos próximos fora da tireoide.
T4a: O tumor é de qualquer tamanho e cresceu extensivamente além da glândula tireoide em tecidos próximos do pescoço, como a laringe, traquéia, esôfago, ou o nervo para a laringe. Isso também é chamado de doença moderadamente avançada .
T4b: O tumor é de qualquer tamanho e cresceu de volta para a espinha ou em grandes vasos sanguíneos próximos. Isso também é chamado de doença muito avançada .
Categorias T para câncer de tireoide anaplásico
Todos os cânceres anaplásicos da tireoide são considerados tumores T4 no momento do diagnóstico.
T4a: O tumor ainda está dentro da tireoide.
T4b: O tumor cresceu fora da tireoide.
Categorias N para o câncer de tireoide
NX: Os gânglios linfáticos regionais (próximos) não podem ser avaliados.
N0: O câncer não se espalhou para os gânglios linfáticos próximos.
N1: O câncer se espalhou para os gânglios linfáticos próximos.
-
N1a: O câncer se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (chamados pré-traqueal , paratraqueal e gânglios linfáticos pré-laríngeos ).
-
N1b: O câncer se espalhou para outros gânglios linfáticos no pescoço (chamado cervical ) ou para os gânglios linfáticos atrás da garganta ( retrofaríngea ) ou no tórax superior ( mediastino superior ).
Categorias M para o câncer de tireoide
MX : A metástase distante não pode ser avaliada.
M0: Não há metástase distante.
M1: O câncer se espalhou para outras partes do corpo, como linfonodos distantes, órgãos internos, ossos, etc.
Agrupamento de estágios
Uma vez que os valores de T, N e M são determinados, eles são combinados em estágios, expressos como um número romano de I a IV. Às vezes as letras são usadas para dividir ainda mais uma fase. Ao contrário da maioria dos outros tipos, os cânceres de tireoide são agrupados em estádios de uma forma que também considera o subtipo de câncer e a idade do paciente.
Câncer de tireoide papilar ou folicular (diferenciado) em pacientes com idade inferior a 45 anos
As pessoas mais jovens têm uma baixa probabilidade de morrer de câncer de tireoide diferenciado (papilar ou folicular). Os agrupamentos de estádio TNM para estes cânceres têm em conta este fato. Assim, todas as pessoas com menos de 45 anos com esses cânceres são estágio I, se eles não têm propagação distante, e estágio II, se eles têm propagação distante.
Estágio I (Qualquer T, Qualquer N, M0): O tumor pode ser de qualquer tamanho (qualquer T) e pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
Estágio II (Qualquer T, Qualquer N, M1): O tumor pode ser de qualquer tamanho (qualquer T) e pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide papilar ou folicular (diferenciado) em pacientes com 45 anos ou mais
Estágio I (T1, N0, M0): O tumor tem 2 cm ou menos e não cresceu fora da tireoide (T1). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio II (T2, N0, M0): O tumor tem mais de 2 cm de diâmetro, mas não tem mais de 4 cm de diâmetro e não cresceu fora da tireoide (T2). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio III: Um dos seguintes se aplica:
T3, N0, M0: O tumor tem mais de 4 cm de diâmetro ou cresceu ligeiramente para fora da tireoide (T3), mas não se espalhou para nódulos linfáticos próximos (N0) ou locais distantes (M0).
T1 a T3, N1a, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da tireoide (T1 a T3). Ele se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (N1a), mas não para outros linfonodos ou para locais distantes (M0).
Estágio IVA: Uma das seguintes opções aplica-se:
T4a, qualquer N, M0: O tumor é de qualquer tamanho e cresceu para além da glândula tireoide e nos tecidos próximos do pescoço (T4a). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
T1 a T3, N1b, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da glândula tireoide (T1 a T3). Ele se espalhou para certos gânglios linfáticos no pescoço (nódulos cervicais) ou para os gânglios linfáticos no tórax superior (nódulos mediastinais superiores) ou atrás da garganta (nódulos retrofaríngeos) (N1b), mas não se espalhou para locais distantes (M0) .
Estágio IVB (T4b, Qualquer N, M0): O tumor tem qualquer tamanho e cresceu de volta para a espinha ou para grandes vasos sanguíneos próximos (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor é de qualquer tamanho e pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide medular
A idade não é um fator no estágio do câncer medular da tireoide.
Estágio I (T1, N0, M0): O tumor tem 2 cm ou menos e não cresceu fora da tireoide (T1). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio II: Uma das seguintes situações aplica-se:
T2, N0, M0: O tumor tem mais de 2 cm mas não tem mais de 4 cm de diâmetro e não cresceu fora da tireoide (T2). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
T3, N0, M0: O tumor é maior que 4 cm ou cresceu ligeiramente fora da tireoide (T3), mas não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio III (T1 a T3, N1a, M0): O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da tireoide (T1 para T3). Ele se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (N1a), mas não para outros linfonodos ou para locais distantes (M0).
Estágio IVA: Uma das seguintes opções aplica-se:
T4a, qualquer N, M0: O tumor é de qualquer tamanho e cresceu para além da glândula da tireoide e nos tecidos próximos do pescoço (T4a). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
T1 a T3, N1b, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da glândula tireoide (T1 a T3). Ele se espalhou para certos gânglios linfáticos no pescoço (nódulos cervicais) ou para os gânglios linfáticos no tórax superior (nódulos mediastinais superiores) ou atrás da garganta (nódulos retrofaríngeos) (N1b), mas não se espalhou para locais distantes (M0) .
Estágio IVB (T4b, Qualquer N, M0): O tumor tem qualquer tamanho e cresceu de volta para a espinha ou para grandes vasos sanguíneos próximos (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor é de qualquer tamanho e pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide anaplásico (indiferenciado)
Todos os cânceres de tireoide anaplásico são considerados estágio IV, refletindo o mau prognóstico deste tipo de câncer.
Estágio IVA (T4a, Qualquer N, M0): O tumor ainda está dentro da tireoide (T4a). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVB (T4b, Qualquer N, M0): O tumor cresceu fora da tiróide (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Recorrente do câncer de tireoide
Esta não é uma etapa real no sistema TNM. O câncer que retorna após o tratamento é chamado de recorrente (ou recaída ). Se o câncer de tireoide retorna, geralmente está no pescoço, mas pode voltar para outra parte do corpo (por exemplo, linfonodos, pulmões ou ossos). Os médicos podem atribuir uma nova fase com base em quão longe o câncer se espalhou, mas isso não é geralmente um processo tão formal como o estadiamento original. A presença de doença recorrente não altera o estadiamento formal original.
Se você tiver alguma dúvida sobre o estágio de seu câncer ou como ele afeta suas opções de tratamento, não se esqueça de perguntar ao seu médico.
Fonte: American Cancer Society
Com formato muito parecido com a de uma borboleta, a glândula tireoide é localizada na parte anterior do pescoço, logo abaixo do Pomo de Adão e é responsável pela produção dos hormônios T3 (triiodotironina) e o T4 (tiroxina) que são essenciais porque interferem em vários controles do organismo, como os batimentos cardíacos, a temperatura, o metabolismo (conjunto de mecanismos químicos necessários ao organismo) que pode ficar mais rápido ou lento, e os movimentos intestinais.
Quais são os tipos de câncer de tireoide?
Carcinoma papilifero – é o mais comum. Pode aparecer em pacientes de qualquer idade, mas é mais freqüente entre 30 e 50 anos. Estima-se que uma a cada mil pessoas tem ou já teve este tipo de câncer. A taxa de cura é alta, chegando a quase 100%.
– Carcinoma folicular – Costuma ocorrer em indivíduos com mais de 40 anos. É mais agressivo do que o papilífero. Em dois terços dos casos, não têm tendência à disseminação. Um tipo de carcinoma folicular mais agressivo é o hurthle, que atinge pessoas com mais de 60 anos.
– Carcinoma medular – Afeta as células parafoliculares, responsáveis pela produção da calcitonia, hormônio que contribui na regulação do nível sanguíneo de cálcio. É de difícil tratamento e, usualmente, se apresenta de moderado a muito agressivo.
– Carcinoma anaplásico ou inmedular – Extremamente raro. Contudo, é do tipo mais agressivo e tem o tratamento mais difícil. É responsável por dois terços dos óbitos de câncer da tireóide.
O que causa o câncer de tireoide e quem está em risco?
A causa exata do câncer de tireoide não é conhecida, mas as pessoas com certos fatores de risco são mais vulneráveis que outras à doença.
Esses fatores de risco incluem:
- tratamentos com radiação para a cabeça, pescoço ou tórax, especialmente na infância ou adolescência
- história familiar de câncer de tireoide
- um grande nódulo ou em rápido crescimento
- idade superior a 40 anos
Ter um fator de risco não significa que você terá câncer de tireoide e algumas pessoas desenvolvem a doença não tem nenhum fator de risco. Ainda assim, ter um nódulo de tireoide com qualquer um desses fatores de risco requer avaliação.
Fonte: ACS
O principal sinal é a aparição de um nódulo indolor na tireoide.
Fonte: ACS
O diagnóstico de câncer na tireoide considera os achados no exame clínico de palpação da glândula e a presença de gânglios linfáticos aumentados. Entretanto, como apenas pequeno número de nódulos é palpável, exames de imagem como a ultrassonografia, a cintilografia e a ressonância magnética são recursos úteis para o diagnóstico. O mais importante, porém, é a biopsia de aspiração com agulha fina para identificar a presença ou não de células tumorais malignas.
Fonte: ACS
Em geral, o tratamento do câncer de tireoide é cirúrgico (tireoidectomia total ou parcial) e leva em conta o tipo e a gravidade da doença. Caso as células malignas tenham comprometido os gânglios cervicais, é necessário retirá-los.
Rouquidão e queda de cálcio são complicações da tireoidectomia associadas a lesões de estruturas como os nervos laríngeos e as glândulas paratireoides respectivamente durante a cirurgia.
Depois de quatro a seis semanas da intervenção, o paciente recebe doses terapêuticas de iodo radioativo em ambiente hospitalar para extinguir qualquer tecido remanescente de células tumorais no corpo e evitar metástases. Quando os carcinomas papilíferos e foliculares não respondem a esse tratamento, é possível recorrer à terapêutica antiangiogênica que consiste em bloquear a formação de novos vasos sanguíneos para impedir que as células tumorais recebam nutrientes e oxigênio através da circulação. O passo seguinte é indicar a reposição hormonal com levotiroxina por via oral para substituir os hormônios que deixaram de ser produzidos pela tireoide. Radioterapia, associada ou não à quimioterapia, é recomendada na ocorrência de tumores mais agressivos, como o carcinoma medular e o carcinoma anaplásico.
Fonte: ACS
É preciso que o médico e o paciente estejam sempre atentos ao estadiamento da doença! Mas, o que é estadiamento? São os estágios que o câncer está no momento, ou seja, o tamanho, a localização e se espalhou para outros órgãos. O estádio de um tumor reflete não apenas a taxa de crescimento e a extensão da doença, mas também o tipo de tumor e sua relação com o hospedeiro. O sistema de estadiamento mais utilizado é o TNM da American Joint Committee on Cancer.
O que é TNM?
É a abreviatura de tumor, linfonodo e metástase. Este sistema utiliza três critérios para avaliar o estágio do câncer:
-
O próprio tumor ( T + um número de 0 a 4 usa-se para descrever o tumor primário);
-
Os linfonodos regionais ao redor do tumor ( N + 0 a 3 usa-se para descrever se a doença disseminou para os gânglios linfáticos)
-
E se o tumor se espalhou para outras partes do corpo (M usa-se para descrever que a doença se espalhou para outros órgãos)
O estadiamento pode ser clínico e patológico. O estadiamento clínico é estabelecido a partir dos dados do exame físico e dos exames complementares. O estadiamento patológico baseia-se nos achados cirúrgicos e no exame anátomopatológico – é estabelecido após tratamento cirúrgico e determina a extensão da doença com maior precisão. Lembrando que o estadiamento patológico pode ou não coincidir com o estadiamento clínico e não é aplicável a todos os tumores.
E o estadiamento do câncer da TIREOIDE, como funciona?
Categorias T para o câncer de tiróide (exceto o câncer anaplásico de tireoide)
TX: O tumor primário não pode ser avaliado.
T0: Nenhuma evidência de tumor primário.
T1: O tumor é de 2 cm (um pouco menos de uma polegada) em toda ou menor e não cresceu fora da tireoide.
-
T1a: O tumor tem 1 cm de diâmetro ou menos e não cresceu fora da tireoide.
-
T1b: O tumor é maior do que 1 cm mas não maior do que 2 cm de diâmetro e não cresceu fora da tireoide.
T2: O tumor tem mais de 2 cm de diâmetro, mas não mais de 4 cm e não cresceu fora da tireoide.
T3: O tumor é maior que 4 cm de diâmetro, ou apenas começou a crescer em tecidos próximos fora da tireoide.
T4a: O tumor é de qualquer tamanho e cresceu extensivamente além da glândula tireoide em tecidos próximos do pescoço, como a laringe, traquéia, esôfago, ou o nervo para a laringe. Isso também é chamado de doença moderadamente avançada .
T4b: O tumor é de qualquer tamanho e cresceu de volta para a espinha ou em grandes vasos sanguíneos próximos. Isso também é chamado de doença muito avançada .
Categorias T para câncer de tireoide anaplásico
Todos os cânceres anaplásicos da tireoide são considerados tumores T4 no momento do diagnóstico.
T4a: O tumor ainda está dentro da tireoide.
T4b: O tumor cresceu fora da tireoide.
Categorias N para o câncer de tireoide
NX: Os gânglios linfáticos regionais (próximos) não podem ser avaliados.
N0: O câncer não se espalhou para os gânglios linfáticos próximos.
N1: O câncer se espalhou para os gânglios linfáticos próximos.
-
N1a: O câncer se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (chamados pré-traqueal , paratraqueal e gânglios linfáticos pré-laríngeos ).
-
N1b: O câncer se espalhou para outros gânglios linfáticos no pescoço (chamado cervical ) ou para os gânglios linfáticos atrás da garganta ( retrofaríngea ) ou no tórax superior ( mediastino superior ).
Categorias M para o câncer de tireoide
MX : A metástase distante não pode ser avaliada.
M0: Não há metástase distante.
M1: O câncer se espalhou para outras partes do corpo, como linfonodos distantes, órgãos internos, ossos, etc.
Agrupamento de estágios
Uma vez que os valores de T, N e M são determinados, eles são combinados em estágios, expressos como um número romano de I a IV. Às vezes as letras são usadas para dividir ainda mais uma fase. Ao contrário da maioria dos outros tipos, os cânceres de tireoide são agrupados em estádios de uma forma que também considera o subtipo de câncer e a idade do paciente.
Câncer de tireoide papilar ou folicular (diferenciado) em pacientes com idade inferior a 45 anos
As pessoas mais jovens têm uma baixa probabilidade de morrer de câncer de tireoide diferenciado (papilar ou folicular). Os agrupamentos de estádio TNM para estes cânceres têm em conta este fato. Assim, todas as pessoas com menos de 45 anos com esses cânceres são estágio I, se eles não têm propagação distante, e estágio II, se eles têm propagação distante.
Estágio I (Qualquer T, Qualquer N, M0): O tumor pode ser de qualquer tamanho (qualquer T) e pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
Estágio II (Qualquer T, Qualquer N, M1): O tumor pode ser de qualquer tamanho (qualquer T) e pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide papilar ou folicular (diferenciado) em pacientes com 45 anos ou mais
Estágio I (T1, N0, M0): O tumor tem 2 cm ou menos e não cresceu fora da tireoide (T1). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio II (T2, N0, M0): O tumor tem mais de 2 cm de diâmetro, mas não tem mais de 4 cm de diâmetro e não cresceu fora da tireoide (T2). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio III: Um dos seguintes se aplica:
T3, N0, M0: O tumor tem mais de 4 cm de diâmetro ou cresceu ligeiramente para fora da tireoide (T3), mas não se espalhou para nódulos linfáticos próximos (N0) ou locais distantes (M0).
T1 a T3, N1a, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da tireoide (T1 a T3). Ele se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (N1a), mas não para outros linfonodos ou para locais distantes (M0).
Estágio IVA: Uma das seguintes opções aplica-se:
T4a, qualquer N, M0: O tumor é de qualquer tamanho e cresceu para além da glândula tireoide e nos tecidos próximos do pescoço (T4a). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
T1 a T3, N1b, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da glândula tireoide (T1 a T3). Ele se espalhou para certos gânglios linfáticos no pescoço (nódulos cervicais) ou para os gânglios linfáticos no tórax superior (nódulos mediastinais superiores) ou atrás da garganta (nódulos retrofaríngeos) (N1b), mas não se espalhou para locais distantes (M0) .
Estágio IVB (T4b, Qualquer N, M0): O tumor tem qualquer tamanho e cresceu de volta para a espinha ou para grandes vasos sanguíneos próximos (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor é de qualquer tamanho e pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide medular
A idade não é um fator no estágio do câncer medular da tireoide.
Estágio I (T1, N0, M0): O tumor tem 2 cm ou menos e não cresceu fora da tireoide (T1). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio II: Uma das seguintes situações aplica-se:
T2, N0, M0: O tumor tem mais de 2 cm mas não tem mais de 4 cm de diâmetro e não cresceu fora da tireoide (T2). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
T3, N0, M0: O tumor é maior que 4 cm ou cresceu ligeiramente fora da tireoide (T3), mas não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio III (T1 a T3, N1a, M0): O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da tireoide (T1 para T3). Ele se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (N1a), mas não para outros linfonodos ou para locais distantes (M0).
Estágio IVA: Uma das seguintes opções aplica-se:
T4a, qualquer N, M0: O tumor é de qualquer tamanho e cresceu para além da glândula da tireoide e nos tecidos próximos do pescoço (T4a). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
T1 a T3, N1b, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da glândula tireoide (T1 a T3). Ele se espalhou para certos gânglios linfáticos no pescoço (nódulos cervicais) ou para os gânglios linfáticos no tórax superior (nódulos mediastinais superiores) ou atrás da garganta (nódulos retrofaríngeos) (N1b), mas não se espalhou para locais distantes (M0) .
Estágio IVB (T4b, Qualquer N, M0): O tumor tem qualquer tamanho e cresceu de volta para a espinha ou para grandes vasos sanguíneos próximos (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor é de qualquer tamanho e pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide anaplásico (indiferenciado)
Todos os cânceres de tireoide anaplásico são considerados estágio IV, refletindo o mau prognóstico deste tipo de câncer.
Estágio IVA (T4a, Qualquer N, M0): O tumor ainda está dentro da tireoide (T4a). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVB (T4b, Qualquer N, M0): O tumor cresceu fora da tiróide (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Recorrente do câncer de tireoide
Esta não é uma etapa real no sistema TNM. O câncer que retorna após o tratamento é chamado de recorrente (ou recaída ). Se o câncer de tireoide retorna, geralmente está no pescoço, mas pode voltar para outra parte do corpo (por exemplo, linfonodos, pulmões ou ossos). Os médicos podem atribuir uma nova fase com base em quão longe o câncer se espalhou, mas isso não é geralmente um processo tão formal como o estadiamento original. A presença de doença recorrente não altera o estadiamento formal original.
Se você tiver alguma dúvida sobre o estágio de seu câncer ou como ele afeta suas opções de tratamento, não se esqueça de perguntar ao seu médico.
Fonte: American Cancer Society
- O que é?
-
Com formato muito parecido com a de uma borboleta, a glândula tireoide é localizada na parte anterior do pescoço, logo abaixo do Pomo de Adão e é responsável pela produção dos hormônios T3 (triiodotironina) e o T4 (tiroxina) que são essenciais porque interferem em vários controles do organismo, como os batimentos cardíacos, a temperatura, o metabolismo (conjunto de mecanismos químicos necessários ao organismo) que pode ficar mais rápido ou lento, e os movimentos intestinais.
Quais são os tipos de câncer de tireoide?
Carcinoma papilifero – é o mais comum. Pode aparecer em pacientes de qualquer idade, mas é mais freqüente entre 30 e 50 anos. Estima-se que uma a cada mil pessoas tem ou já teve este tipo de câncer. A taxa de cura é alta, chegando a quase 100%.
– Carcinoma folicular – Costuma ocorrer em indivíduos com mais de 40 anos. É mais agressivo do que o papilífero. Em dois terços dos casos, não têm tendência à disseminação. Um tipo de carcinoma folicular mais agressivo é o hurthle, que atinge pessoas com mais de 60 anos.
– Carcinoma medular – Afeta as células parafoliculares, responsáveis pela produção da calcitonia, hormônio que contribui na regulação do nível sanguíneo de cálcio. É de difícil tratamento e, usualmente, se apresenta de moderado a muito agressivo.
– Carcinoma anaplásico ou inmedular – Extremamente raro. Contudo, é do tipo mais agressivo e tem o tratamento mais difícil. É responsável por dois terços dos óbitos de câncer da tireóide.
- Fatores de Risco
-
O que causa o câncer de tireoide e quem está em risco?
A causa exata do câncer de tireoide não é conhecida, mas as pessoas com certos fatores de risco são mais vulneráveis que outras à doença.
Esses fatores de risco incluem:
- tratamentos com radiação para a cabeça, pescoço ou tórax, especialmente na infância ou adolescência
- história familiar de câncer de tireoide
- um grande nódulo ou em rápido crescimento
- idade superior a 40 anos
Ter um fator de risco não significa que você terá câncer de tireoide e algumas pessoas desenvolvem a doença não tem nenhum fator de risco. Ainda assim, ter um nódulo de tireoide com qualquer um desses fatores de risco requer avaliação.
Fonte: ACS
- Sintomas
-
O principal sinal é a aparição de um nódulo indolor na tireoide.
Fonte: ACS
- Diagnóstico
-
O diagnóstico de câncer na tireoide considera os achados no exame clínico de palpação da glândula e a presença de gânglios linfáticos aumentados. Entretanto, como apenas pequeno número de nódulos é palpável, exames de imagem como a ultrassonografia, a cintilografia e a ressonância magnética são recursos úteis para o diagnóstico. O mais importante, porém, é a biopsia de aspiração com agulha fina para identificar a presença ou não de células tumorais malignas.
Fonte: ACS
- Tratamento
-
Em geral, o tratamento do câncer de tireoide é cirúrgico (tireoidectomia total ou parcial) e leva em conta o tipo e a gravidade da doença. Caso as células malignas tenham comprometido os gânglios cervicais, é necessário retirá-los.
Rouquidão e queda de cálcio são complicações da tireoidectomia associadas a lesões de estruturas como os nervos laríngeos e as glândulas paratireoides respectivamente durante a cirurgia.
Depois de quatro a seis semanas da intervenção, o paciente recebe doses terapêuticas de iodo radioativo em ambiente hospitalar para extinguir qualquer tecido remanescente de células tumorais no corpo e evitar metástases. Quando os carcinomas papilíferos e foliculares não respondem a esse tratamento, é possível recorrer à terapêutica antiangiogênica que consiste em bloquear a formação de novos vasos sanguíneos para impedir que as células tumorais recebam nutrientes e oxigênio através da circulação. O passo seguinte é indicar a reposição hormonal com levotiroxina por via oral para substituir os hormônios que deixaram de ser produzidos pela tireoide. Radioterapia, associada ou não à quimioterapia, é recomendada na ocorrência de tumores mais agressivos, como o carcinoma medular e o carcinoma anaplásico.
Fonte: ACS
- Estadiamento
-
É preciso que o médico e o paciente estejam sempre atentos ao estadiamento da doença! Mas, o que é estadiamento? São os estágios que o câncer está no momento, ou seja, o tamanho, a localização e se espalhou para outros órgãos. O estádio de um tumor reflete não apenas a taxa de crescimento e a extensão da doença, mas também o tipo de tumor e sua relação com o hospedeiro. O sistema de estadiamento mais utilizado é o TNM da American Joint Committee on Cancer.
O que é TNM?
É a abreviatura de tumor, linfonodo e metástase. Este sistema utiliza três critérios para avaliar o estágio do câncer:
-
O próprio tumor ( T + um número de 0 a 4 usa-se para descrever o tumor primário);
-
Os linfonodos regionais ao redor do tumor ( N + 0 a 3 usa-se para descrever se a doença disseminou para os gânglios linfáticos)
-
E se o tumor se espalhou para outras partes do corpo (M usa-se para descrever que a doença se espalhou para outros órgãos)
O estadiamento pode ser clínico e patológico. O estadiamento clínico é estabelecido a partir dos dados do exame físico e dos exames complementares. O estadiamento patológico baseia-se nos achados cirúrgicos e no exame anátomopatológico – é estabelecido após tratamento cirúrgico e determina a extensão da doença com maior precisão. Lembrando que o estadiamento patológico pode ou não coincidir com o estadiamento clínico e não é aplicável a todos os tumores.
E o estadiamento do câncer da TIREOIDE, como funciona?
Categorias T para o câncer de tiróide (exceto o câncer anaplásico de tireoide)
TX: O tumor primário não pode ser avaliado.
T0: Nenhuma evidência de tumor primário.
T1: O tumor é de 2 cm (um pouco menos de uma polegada) em toda ou menor e não cresceu fora da tireoide.
-
T1a: O tumor tem 1 cm de diâmetro ou menos e não cresceu fora da tireoide.
-
T1b: O tumor é maior do que 1 cm mas não maior do que 2 cm de diâmetro e não cresceu fora da tireoide.
T2: O tumor tem mais de 2 cm de diâmetro, mas não mais de 4 cm e não cresceu fora da tireoide.
T3: O tumor é maior que 4 cm de diâmetro, ou apenas começou a crescer em tecidos próximos fora da tireoide.
T4a: O tumor é de qualquer tamanho e cresceu extensivamente além da glândula tireoide em tecidos próximos do pescoço, como a laringe, traquéia, esôfago, ou o nervo para a laringe. Isso também é chamado de doença moderadamente avançada .
T4b: O tumor é de qualquer tamanho e cresceu de volta para a espinha ou em grandes vasos sanguíneos próximos. Isso também é chamado de doença muito avançada .
Categorias T para câncer de tireoide anaplásico
Todos os cânceres anaplásicos da tireoide são considerados tumores T4 no momento do diagnóstico.
T4a: O tumor ainda está dentro da tireoide.
T4b: O tumor cresceu fora da tireoide.
Categorias N para o câncer de tireoide
NX: Os gânglios linfáticos regionais (próximos) não podem ser avaliados.
N0: O câncer não se espalhou para os gânglios linfáticos próximos.
N1: O câncer se espalhou para os gânglios linfáticos próximos.
-
N1a: O câncer se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (chamados pré-traqueal , paratraqueal e gânglios linfáticos pré-laríngeos ).
-
N1b: O câncer se espalhou para outros gânglios linfáticos no pescoço (chamado cervical ) ou para os gânglios linfáticos atrás da garganta ( retrofaríngea ) ou no tórax superior ( mediastino superior ).
Categorias M para o câncer de tireoide
MX : A metástase distante não pode ser avaliada.
M0: Não há metástase distante.
M1: O câncer se espalhou para outras partes do corpo, como linfonodos distantes, órgãos internos, ossos, etc.
Agrupamento de estágios
Uma vez que os valores de T, N e M são determinados, eles são combinados em estágios, expressos como um número romano de I a IV. Às vezes as letras são usadas para dividir ainda mais uma fase. Ao contrário da maioria dos outros tipos, os cânceres de tireoide são agrupados em estádios de uma forma que também considera o subtipo de câncer e a idade do paciente.
Câncer de tireoide papilar ou folicular (diferenciado) em pacientes com idade inferior a 45 anos
As pessoas mais jovens têm uma baixa probabilidade de morrer de câncer de tireoide diferenciado (papilar ou folicular). Os agrupamentos de estádio TNM para estes cânceres têm em conta este fato. Assim, todas as pessoas com menos de 45 anos com esses cânceres são estágio I, se eles não têm propagação distante, e estágio II, se eles têm propagação distante.
Estágio I (Qualquer T, Qualquer N, M0): O tumor pode ser de qualquer tamanho (qualquer T) e pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
Estágio II (Qualquer T, Qualquer N, M1): O tumor pode ser de qualquer tamanho (qualquer T) e pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide papilar ou folicular (diferenciado) em pacientes com 45 anos ou mais
Estágio I (T1, N0, M0): O tumor tem 2 cm ou menos e não cresceu fora da tireoide (T1). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio II (T2, N0, M0): O tumor tem mais de 2 cm de diâmetro, mas não tem mais de 4 cm de diâmetro e não cresceu fora da tireoide (T2). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio III: Um dos seguintes se aplica:
T3, N0, M0: O tumor tem mais de 4 cm de diâmetro ou cresceu ligeiramente para fora da tireoide (T3), mas não se espalhou para nódulos linfáticos próximos (N0) ou locais distantes (M0).
T1 a T3, N1a, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da tireoide (T1 a T3). Ele se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (N1a), mas não para outros linfonodos ou para locais distantes (M0).
Estágio IVA: Uma das seguintes opções aplica-se:
T4a, qualquer N, M0: O tumor é de qualquer tamanho e cresceu para além da glândula tireoide e nos tecidos próximos do pescoço (T4a). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
T1 a T3, N1b, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da glândula tireoide (T1 a T3). Ele se espalhou para certos gânglios linfáticos no pescoço (nódulos cervicais) ou para os gânglios linfáticos no tórax superior (nódulos mediastinais superiores) ou atrás da garganta (nódulos retrofaríngeos) (N1b), mas não se espalhou para locais distantes (M0) .
Estágio IVB (T4b, Qualquer N, M0): O tumor tem qualquer tamanho e cresceu de volta para a espinha ou para grandes vasos sanguíneos próximos (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor é de qualquer tamanho e pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide medular
A idade não é um fator no estágio do câncer medular da tireoide.
Estágio I (T1, N0, M0): O tumor tem 2 cm ou menos e não cresceu fora da tireoide (T1). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio II: Uma das seguintes situações aplica-se:
T2, N0, M0: O tumor tem mais de 2 cm mas não tem mais de 4 cm de diâmetro e não cresceu fora da tireoide (T2). Não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
T3, N0, M0: O tumor é maior que 4 cm ou cresceu ligeiramente fora da tireoide (T3), mas não se espalhou para os nódulos linfáticos próximos (N0) ou locais distantes (M0).
Estágio III (T1 a T3, N1a, M0): O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da tireoide (T1 para T3). Ele se espalhou para os gânglios linfáticos ao redor da tireoide no pescoço (N1a), mas não para outros linfonodos ou para locais distantes (M0).
Estágio IVA: Uma das seguintes opções aplica-se:
T4a, qualquer N, M0: O tumor é de qualquer tamanho e cresceu para além da glândula da tireoide e nos tecidos próximos do pescoço (T4a). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Não se espalhou para locais distantes (M0).
T1 a T3, N1b, M0: O tumor é de qualquer tamanho e pode ter crescido ligeiramente fora da glândula tireoide (T1 a T3). Ele se espalhou para certos gânglios linfáticos no pescoço (nódulos cervicais) ou para os gânglios linfáticos no tórax superior (nódulos mediastinais superiores) ou atrás da garganta (nódulos retrofaríngeos) (N1b), mas não se espalhou para locais distantes (M0) .
Estágio IVB (T4b, Qualquer N, M0): O tumor tem qualquer tamanho e cresceu de volta para a espinha ou para grandes vasos sanguíneos próximos (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor é de qualquer tamanho e pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Câncer de tireoide anaplásico (indiferenciado)
Todos os cânceres de tireoide anaplásico são considerados estágio IV, refletindo o mau prognóstico deste tipo de câncer.
Estágio IVA (T4a, Qualquer N, M0): O tumor ainda está dentro da tireoide (T4a). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVB (T4b, Qualquer N, M0): O tumor cresceu fora da tiróide (T4b). Pode ou não ter se espalhado para os nódulos linfáticos próximos (qualquer N), mas não se espalhou para locais distantes (M0).
Estágio IVC (Qualquer T, Qualquer N, M1): O tumor pode ou não ter crescido fora da tireoide (qualquer T). Pode ou não ter se espalhado para os gânglios linfáticos próximos (qualquer N). Ele se espalhou para locais distantes (M1).
Recorrente do câncer de tireoide
Esta não é uma etapa real no sistema TNM. O câncer que retorna após o tratamento é chamado de recorrente (ou recaída ). Se o câncer de tireoide retorna, geralmente está no pescoço, mas pode voltar para outra parte do corpo (por exemplo, linfonodos, pulmões ou ossos). Os médicos podem atribuir uma nova fase com base em quão longe o câncer se espalhou, mas isso não é geralmente um processo tão formal como o estadiamento original. A presença de doença recorrente não altera o estadiamento formal original.
Se você tiver alguma dúvida sobre o estágio de seu câncer ou como ele afeta suas opções de tratamento, não se esqueça de perguntar ao seu médico.
Fonte: American Cancer Society
-
Doenças autoimunes são doenças que atacam o sistema imunológico contra uma estrutura do próprio organismo, ou seja, uma resposta autoimune. Todo mundo aprende na escola que o sistema imunológico existe para combater ameaças externas, como vírus e bactérias. Ao “visualizar” esses agentes, produz anticorpos com o objetivo de atacá-los. Em alguns casos, no entanto, o general desse exército confunde células do próprio organismo com invasores.
Os mecanismos imunológicos que ocasionam a lesão dos órgãos nessas doenças é algo que médicos e cientistas até compreendem bem. Já o que leva o sistema imunológico a se reverter, destruindo algo que teoricamente deveria ser protegido, ainda é um mistério, ou “a pergunta que vale um bilhão de dólares”, como diz o médico Freddy Eliaschewitz, consultor da ADJ Diabetes Brasil.
De acordo com o Instituto Nacional de Saúde (NIH), dos EUA, mais de uma centena de doenças crônicas têm origem em uma resposta autoimune. Mas, apesar do processo em comum, cada doença autoimune tem suas próprias características, ritmo evolutivo e sintomas específicos. É por isso que não existe um médico especialista em “autoimunidade”.
“Hoje sabe-se que existe até infertilidade causada por doença autoimune, ou seja, é algo que permeia toda a medicina”, explica o reumatologista Luís Eduardo Coelho Andrade, professor da Universidade Federal de São Paulo. Mas, endocrinologistas, dermatologistas e diversos outros especialistas podem ser requisitados, bem como outros profissionais de saúde, como nutricionistas, psicólogos e fisioterapeutas.
Embora existam diversas teorias para explicar a autoimunidade, é importante frisar que nenhuma delas foi confirmada até hoje, segundo os especialistas. A “teoria da higiene” é uma delas – como as doenças são mais comuns em países mais desenvolvidos e em áreas urbanas, cogita-se que o consumo de alimentos pasteurizados e o excesso de higiene estariam impedindo o sistema imunológico dessas populações de se “educar” corretamente.
Outra teoria é a do mimetismo molecular – alguns micro-organismos teriam aumentado suas chances de sobrevivência com a capacidade de se camuflar dentro do organismo. Essa semelhança faria o sistema imunológico se confundir e passar a combater uma estrutura própria depois de uma virose, por exemplo. Há, ainda, a ideia de que certas infecções levariam o organismo a expor componentes que antes ficavam escondidos e, portanto, não são reconhecidos pelo sistema imunológico.
DADOS DOENÇAS AUTOIMUNES
Estima-se que as doenças autoimunes afetem de 5 a 8% da população geral. Considerando cada doença autoimune especificamente, a frequência é bem menor, variando de 0,01 a 1%, mas há estimativas menos otimistas. Os Institutos Nacionais de Saúde dos EUA, por exemplo, afirmam que 23,5 milhões de norte-americanos sofrem dessas enfermidades, o que não é pouco para uma população de cerca de 320 milhões. Já a American Autoimmune Related Diseases Association (AARDA), uma entidade sem fins lucrativos, diz que 50 milhões é um número mais realista, pois os Institutos só consideram 24 doenças para as quais há pesquisas epidemiológicas de qualidade. Só para se ter uma ideia do que essa estimativa representa: as doenças cardíacas afetam cerca de 22 milhões de norte-americanos e o câncer, 9 milhões. É preciso haver uma tendência genética para desenvolver essas doenças. Segundo os especialistas, existem variantes genéticas conhecidas que predispõem parte da população às doenças autoimunes. Ou seja, algumas pessoas nunca vão desenvolver o problema, enquanto algumas famílias podem ter diversos membros com diferentes tipos de doenças autoimunes. Mas ter a tendência não significa ter a enfermidade – é preciso que haja um fator ambiental que deflagre a doença.
Aproximadamente 75% das pessoas que sofrem de doenças autoimunes são mulheres. A justificativa mais aceitável para essa desigualdade é o fator hormonal: “O estrógeno é um estimulante da imunidade”, explica o reumatologista da Unifesp. Tanto que boa parte das doenças autoimunes acomete mulheres em idade fértil.
QUAIS OS PRINCIPAIS SINTOMAS?
Embora toda doença autoimune seja crônica, algumas pessoas apresentam sintomas mais leves, enquanto outras têm manifestações tão intensas que, em certos casos, podem levar à morte. Um dos exemplos é o lúpus: enquanto alguns pacientes apresentam eventuais dores nas articulações e a famosa mancha no rosto, em forma de borboleta, outros desenvolvem problemas sérios nos rins ou nos vasos sanguíneos (vasculite).
COMO FUNCIONA O TRATAMENTO?
O tratamento para doenças autoimunes evoluiu bastante nos últimos anos e varia de acordo com a enfermidade, mas o uso de corticoides é algo frequente. Esses anti-inflamatórios são eficazes e ajudam a controlar a reação do organismo, mas seu uso crônico traz efeitos indesejados, como aumento da vulnerabilidade a infecções e ganho de peso.
“Hoje há novos remédios que permitem um uso menor de corticoide”, informa Andrade. E alguns medicamentos biológicos, derivados da biotecnologia, têm sido bastante eficazes no caso de certas doenças, como artrite reumatoide, psoríase e doença de Crohn, embora o custo ainda seja muito alto.
O reumatologista da Unifesp conta que ele próprio, em sua experiência pessoal, presenciou um avanço notável nos últimos anos. “Antigamente, os ambulatórios para artrite reumatoide eram lotados de cadeiras de rodas, e hoje você encontra uma ou outra”, relata. “E se antes dar o diagnóstico de lúpus a uma garota de 20 anos era uma sentença, hoje você pode dizer à paciente que ela terá uma vida normal, só terá que ser mais disciplinada com exames, consultas e medicamentos.”
Existem pesquisas experimentais com terapias que, de alguma forma, ajudariam a “resetar” o sistema imunológico. É o caso, por exemplo, do uso de células-tronco na tentativa de combater o diabetes tipo 1. Mas ainda há muitos obstáculos a serem enfrentados. Freddy Eliaschewitz comenta que muitos pacientes entram em remissão, mas depois a doença volta a se manifestar. E um procedimento desse tipo sempre envolve riscos, pois são necessárias altas doses de imunossupressores.
Quando se fala em doença autoimune, um dos exames mais lembrados é o FAN (Fator Antinúcleo). Ele é realizado para detectar autoanticorpos (são anticorpos dirigidos para células e tecidos do próprio corpo) contra estruturas nucleares das células e costuma ser solicitado quando há suspeita de reações autoimunes, por exemplo, a presença de dores articulares sem lesões ou desgaste aparentes. Há vários padrões analisados, e, cada um deles, quando o resultado é positivo, pode ser sugestivo de uma ou outra doença autoimune.
Luís Eduardo Andrade explica que o FAN foi muito importante quando se iniciaram os diagnósticos de autoimunidade, a partir da metade do século passado. Mas, depois, os cientistas descobriram que muitos indivíduos saudáveis, ou com certas infecções, também podem apresentar o exame positivo. Portanto, o FAN pode ajudar a estabelecer um diagnóstico que tenha surgido a partir de sintomas, mas, sozinho, não significa nada.
Em geral, diante da suspeita de doença autoimune, o médico solicita também outros exames de sangue para identificar anticorpos específicos.
Existe relação entre estresse e doença autoimune?
Muitos pacientes contam que tiveram uma doença autoimune deflagrada depois de sofrer algum evento traumático. De acordo com o reumatologista da Unifesp, essa relação com o emocional é observada em alguns indivíduos, mas é difícil medir esse tipo de impacto de forma consistente.
Mas o médico avisa que o estresse pode influenciar, sim, o estado da doença. Por isso é importante que os pacientes diagnosticados busquem ter uma vida equilibrada, com atividade física, nutrição adequada e sono suficiente. “Há conexões importantes entre o sistema nervoso e o sistema imunológico”, justifica.
Doenças
São doenças de longa duração e de progressão lenta, e muitas, infelizmente, ainda não tem cura. Existem duas categorias de doenças crônicas: as transmissíveis e as não transmissíveis (DCNT).
As doenças crônicas não transmissíveis estão associadas a idade elevada ou ao estilo de vida da pessoa, como má alimentação, estresse e sedentarismo. Como por exemplo doenças respiratórias (asma, bronquite, Doenças Pulmonar Obstrutivas Crônica – DPOC etc), doenças metabólicas (obesidade, diabetes, hiper e hipotireoidismo, dislipidemia, etc), entre outras.
Já as doenças crônicas transmissíveis são infecciosas e causadas por organismos invasores como vírus e parasitas. Exemplos deste tipo de doença: AIDS, hepatite B e C e tuberculose.
DADOS DOENÇAS CRÔNICAS
Segundo a Agência Nacional de Saúde (ANS), existem, somente no Brasil, quase 53 milhões de pessoas com pelo menos uma doença crônica. Estima-se que até 2030 teremos um aumento de 50% da população com algum tipo de doença crônica, por conta do atual estilo de vida: obesidade, sedentarismo e estresse, de acordo com a Organização Mundial da Saúde. De acordo com o Instituto Brasileiro de Geografia e Estatística/IBGE, as doenças crônicas não transmissíveis representam 70% das mortes no Brasil.
EXISTE PREVENÇÃO PARA DOENÇAS CRÔNICAS?
Sabe-se que tudo na vida precisa ser a base do equilíbrio, e com as doenças não poderia ser diferente. Um estilo de vida saudável, buscando a alimentação adequada, a prática de algum exercício físico e cuidar da sua mente, são fatores essenciais para a prevenção de qualquer doença. Preste bem atenção: essas variáveis modificáveis ajudam na prevenção e melhoram a qualidade de vida de qualquer pessoa, porém não pode-se afirmar que a pessoa que tem um ótimo estilo de vida, não terá nenhuma doença crônica.
Doenças
O Câncer de Vagina é um tipo raro de câncer que ocorre no sistema reprodutor feminino e, segundo estatísticas, atinge, geralmente, mulheres entre os 45 e 65 anos, ou mulheres que não mantêm relação sexual. . Na maior parte dos casos o câncer de vagina é de origem secundária, ou seja, proveniente de metástases de câncer em órgãos próximos, como o de colo de útero, ovários, endométrio ou até de intestino grosso. O Carcinoma Epidermoide, câncer na vagina causado pelas células da própria vagina, são apenas 1% de cânceres ginecológicos.
Alguns fatores podem aumentar o risco de câncer de vagina como:
- Idade
- Tabagismo
- Alcoolismo
- Adenose Vaginal
- HPV (Vírus do Papiloma Humano)
- HIV (Vírus da Imunodeficiência Humana) – Virus que causa a AIDS
- Câncer de Colo do Útero
- Irritação na vagina
- Não manter relações sexuais (já que alguns sintomas, como dor durante o sexo, por exemplo, podem não ser percebidos)
Grande parte das mulheres com câncer vaginal apresentam sintomas como:
- Corrimento vaginal anormal com cheiro;
- Sangramento vaginal anormal – fora do período menstrual;
- Dor durante as relações sexuais;
- Sangramento após a relação sexual;
- Ardência;
- Ulcerações (feridas) com infecção ou não;
- Urgência em urinar;
- Dor ou ardência ao urinar;
- Dor pélvica;
- Prisão de ventre;
- Massa palpável
Os principais exames para diagnosticar o câncer de vagina são o Papanicolau e a Colposcopia, que permite examinar a olho nu ou com o aparelho colposcópio lesões ou problemas possíveis. Lesões suspeitas poderão passar por biópsia para um diagnóstico mais preciso. Outros exames podem ser usados também como exames de imagem (Radiografia do Torax, Tomografia Computadorizada, Ressonância Magnética e PETscan).
O tratamento varia conforme o estagio da doença e danos causados, mas os principais métodos são:
- Cirurgia – para retirada dos tecidos comprometidos pela doença;
- Radioterapia;
- Quimioterapia
Em atualização.
O Câncer de Vagina é um tipo raro de câncer que ocorre no sistema reprodutor feminino e, segundo estatísticas, atinge, geralmente, mulheres entre os 45 e 65 anos, ou mulheres que não mantêm relação sexual. . Na maior parte dos casos o câncer de vagina é de origem secundária, ou seja, proveniente de metástases de câncer em órgãos próximos, como o de colo de útero, ovários, endométrio ou até de intestino grosso. O Carcinoma Epidermoide, câncer na vagina causado pelas células da própria vagina, são apenas 1% de cânceres ginecológicos.
Alguns fatores podem aumentar o risco de câncer de vagina como:
- Idade
- Tabagismo
- Alcoolismo
- Adenose Vaginal
- HPV (Vírus do Papiloma Humano)
- HIV (Vírus da Imunodeficiência Humana) – Virus que causa a AIDS
- Câncer de Colo do Útero
- Irritação na vagina
- Não manter relações sexuais (já que alguns sintomas, como dor durante o sexo, por exemplo, podem não ser percebidos)
Grande parte das mulheres com câncer vaginal apresentam sintomas como:
- Corrimento vaginal anormal com cheiro;
- Sangramento vaginal anormal – fora do período menstrual;
- Dor durante as relações sexuais;
- Sangramento após a relação sexual;
- Ardência;
- Ulcerações (feridas) com infecção ou não;
- Urgência em urinar;
- Dor ou ardência ao urinar;
- Dor pélvica;
- Prisão de ventre;
- Massa palpável
Os principais exames para diagnosticar o câncer de vagina são o Papanicolau e a Colposcopia, que permite examinar a olho nu ou com o aparelho colposcópio lesões ou problemas possíveis. Lesões suspeitas poderão passar por biópsia para um diagnóstico mais preciso. Outros exames podem ser usados também como exames de imagem (Radiografia do Torax, Tomografia Computadorizada, Ressonância Magnética e PETscan).
O tratamento varia conforme o estagio da doença e danos causados, mas os principais métodos são:
- Cirurgia – para retirada dos tecidos comprometidos pela doença;
- Radioterapia;
- Quimioterapia
Em atualização.
- O que é?
-
O Câncer de Vagina é um tipo raro de câncer que ocorre no sistema reprodutor feminino e, segundo estatísticas, atinge, geralmente, mulheres entre os 45 e 65 anos, ou mulheres que não mantêm relação sexual. . Na maior parte dos casos o câncer de vagina é de origem secundária, ou seja, proveniente de metástases de câncer em órgãos próximos, como o de colo de útero, ovários, endométrio ou até de intestino grosso. O Carcinoma Epidermoide, câncer na vagina causado pelas células da própria vagina, são apenas 1% de cânceres ginecológicos.
- Fatores de Risco
-
Alguns fatores podem aumentar o risco de câncer de vagina como:
- Idade
- Tabagismo
- Alcoolismo
- Adenose Vaginal
- HPV (Vírus do Papiloma Humano)
- HIV (Vírus da Imunodeficiência Humana) – Virus que causa a AIDS
- Câncer de Colo do Útero
- Irritação na vagina
- Não manter relações sexuais (já que alguns sintomas, como dor durante o sexo, por exemplo, podem não ser percebidos)
- Sintomas
-
Grande parte das mulheres com câncer vaginal apresentam sintomas como:
- Corrimento vaginal anormal com cheiro;
- Sangramento vaginal anormal – fora do período menstrual;
- Dor durante as relações sexuais;
- Sangramento após a relação sexual;
- Ardência;
- Ulcerações (feridas) com infecção ou não;
- Urgência em urinar;
- Dor ou ardência ao urinar;
- Dor pélvica;
- Prisão de ventre;
- Massa palpável
- Diagnóstico
-
Os principais exames para diagnosticar o câncer de vagina são o Papanicolau e a Colposcopia, que permite examinar a olho nu ou com o aparelho colposcópio lesões ou problemas possíveis. Lesões suspeitas poderão passar por biópsia para um diagnóstico mais preciso. Outros exames podem ser usados também como exames de imagem (Radiografia do Torax, Tomografia Computadorizada, Ressonância Magnética e PETscan).
- Tratamento
-
O tratamento varia conforme o estagio da doença e danos causados, mas os principais métodos são:
- Cirurgia – para retirada dos tecidos comprometidos pela doença;
- Radioterapia;
- Quimioterapia
- Estadiamento
-
Em atualização.
Fibrilação Atrial é a arritmia sustentada mais comum do mundo ocidental, ocorrendo com frequência cada vez maior à medida que a população envelhece. Uma arritmia isolada ou de ocorrência familial, fibrilação atrial no passado era considerada benigna, mas com o passar dos anos e com a complexidade dos estudos médicos, verificou-se que a fibrilação atrial acompanha ou é causa de muitas morbidades.
Na fibrilação atrial ocorre uma alteração na formação do estímulo cardíaco nos átrios. Ocorre uma espécie de curto circuito em várias áreas dos átrios, gerando inúmeros diminutos estímulos simultânea. Ocasionando uma desorganização elétrica tamanha que o coração torna-se incapaz de gerar a contração dos átrios.
Como há uma filtração importante no nodo sinoatrial, acaba que apenas um estímulo prossegue para os ventrículos por vez. Entretanto, apesar da filtração eficiente há transmissões elétricas descompassadas e rápidas para os ventrículos, ou seja, o coração acaba por bater de forma irregular e acelerada.
Em vez de contraírem, os átrios fibrilam – apresentam um movimento como se fosse um tremor grosseiro. E esta movimentação anômala gera um fluxo irregular do sangue, propiciando a formação de trombos dentro das cavidades cardíacas. Uma vez formados, os trombos podem migrar para os pulmões (gerando embolia pulmonar), para o cérebro (gerando AVC) e para os órgãos periféricos (rins, fígado, intestino, etc…).
Uma observação importância é quanto a incidência, segundo a Sociedade Brasileira de Cardiologia, cerca de um em cada 10 mil jovens brasileiros sem problemas cardiopaticos aparante tem fibrilação atrial. Nesses indivíduos, a doença é geralmente intermitente, mas 25% dos casos pode se tornar uma doença crônica.
O impacto da fibrilação atrial na morbimortalidade da população é elevado, bem como suas consequências socioeconômicas, relacionado, principalmente, a internações hospitalares, manejo crônico da doença e incapacitação ou limitação física de seus portadores, neste caso, mais comumente nos idosos.
A Fibrilação Atrial é uma doença um pouco diferente das que conhecemos, pois não existe uma relação causa-consequência única!
Existem inúmeras possibilidades e elas podem estar atuando ao mesmo tempo em um mesmo indivíduo!
Podemos citar:
- álcool
- tabagismo
- apneia do sono
- doença cardíaca
- hipertensão arterial sistêmica
- diabetes
- entorpecentes
- cirurgias
- obesidade
- histórico familiar
- distúrbios metabólicos
Causas reversíveis de Fibrilação Atrial
Fibrilação Atrial pode ser provocada durante situações transitórias, incluindo a ingestão de álcool, cirurgias, choque elétrico, infarto do miocárdio, pericardite, miocardite, embolia pulmonar, outras doenças pulmonares, hipertireoidismo e outras doenças metabólicas.
Algumas vezes a fibrilação atrial não apresenta sintomas, porém quando surgem, os sintomas mais comuns são:
- Palpitações no peito
- Fraqueza/Fadiga
- Capacidade reduzida de se exercitar
- Tontura
- Confusão
- Falta de ar
- Dor no peito
- Desmaio.
Como é uma arritmia comum, bons clínicos gerais e outros especialistas conseguem identificá-la facilmente, apenas através da palpação e ausculta de um ritmo cardíaco caótico. Mas a documentação através do eletrocardiograma simples, de 12 derivações, é o exame padrão, não sendo necessária nenhuma confirmação diagnóstica complementar. Então o paciente poderá ser encaminhado a um cardiologista, que assim procederá a investigação das causas, estimativa dos riscos e proposta de tratamento.
Existem algumas opções de tratamento para a Fibrilação Atrial como: medicações, cardioversão elétrica (choque elétrico no tórax), ablação por cateter ou cirurgia.
Não há estadiamento.
Fibrilação Atrial é a arritmia sustentada mais comum do mundo ocidental, ocorrendo com frequência cada vez maior à medida que a população envelhece. Uma arritmia isolada ou de ocorrência familial, fibrilação atrial no passado era considerada benigna, mas com o passar dos anos e com a complexidade dos estudos médicos, verificou-se que a fibrilação atrial acompanha ou é causa de muitas morbidades.
Na fibrilação atrial ocorre uma alteração na formação do estímulo cardíaco nos átrios. Ocorre uma espécie de curto circuito em várias áreas dos átrios, gerando inúmeros diminutos estímulos simultânea. Ocasionando uma desorganização elétrica tamanha que o coração torna-se incapaz de gerar a contração dos átrios.
Como há uma filtração importante no nodo sinoatrial, acaba que apenas um estímulo prossegue para os ventrículos por vez. Entretanto, apesar da filtração eficiente há transmissões elétricas descompassadas e rápidas para os ventrículos, ou seja, o coração acaba por bater de forma irregular e acelerada.
Em vez de contraírem, os átrios fibrilam – apresentam um movimento como se fosse um tremor grosseiro. E esta movimentação anômala gera um fluxo irregular do sangue, propiciando a formação de trombos dentro das cavidades cardíacas. Uma vez formados, os trombos podem migrar para os pulmões (gerando embolia pulmonar), para o cérebro (gerando AVC) e para os órgãos periféricos (rins, fígado, intestino, etc…).
Uma observação importância é quanto a incidência, segundo a Sociedade Brasileira de Cardiologia, cerca de um em cada 10 mil jovens brasileiros sem problemas cardiopaticos aparante tem fibrilação atrial. Nesses indivíduos, a doença é geralmente intermitente, mas 25% dos casos pode se tornar uma doença crônica.
O impacto da fibrilação atrial na morbimortalidade da população é elevado, bem como suas consequências socioeconômicas, relacionado, principalmente, a internações hospitalares, manejo crônico da doença e incapacitação ou limitação física de seus portadores, neste caso, mais comumente nos idosos.
A Fibrilação Atrial é uma doença um pouco diferente das que conhecemos, pois não existe uma relação causa-consequência única!
Existem inúmeras possibilidades e elas podem estar atuando ao mesmo tempo em um mesmo indivíduo!
Podemos citar:
- álcool
- tabagismo
- apneia do sono
- doença cardíaca
- hipertensão arterial sistêmica
- diabetes
- entorpecentes
- cirurgias
- obesidade
- histórico familiar
- distúrbios metabólicos
Causas reversíveis de Fibrilação Atrial
Fibrilação Atrial pode ser provocada durante situações transitórias, incluindo a ingestão de álcool, cirurgias, choque elétrico, infarto do miocárdio, pericardite, miocardite, embolia pulmonar, outras doenças pulmonares, hipertireoidismo e outras doenças metabólicas.
Algumas vezes a fibrilação atrial não apresenta sintomas, porém quando surgem, os sintomas mais comuns são:
- Palpitações no peito
- Fraqueza/Fadiga
- Capacidade reduzida de se exercitar
- Tontura
- Confusão
- Falta de ar
- Dor no peito
- Desmaio.
Como é uma arritmia comum, bons clínicos gerais e outros especialistas conseguem identificá-la facilmente, apenas através da palpação e ausculta de um ritmo cardíaco caótico. Mas a documentação através do eletrocardiograma simples, de 12 derivações, é o exame padrão, não sendo necessária nenhuma confirmação diagnóstica complementar. Então o paciente poderá ser encaminhado a um cardiologista, que assim procederá a investigação das causas, estimativa dos riscos e proposta de tratamento.
Existem algumas opções de tratamento para a Fibrilação Atrial como: medicações, cardioversão elétrica (choque elétrico no tórax), ablação por cateter ou cirurgia.
Não há estadiamento.
- O que é?
-
Fibrilação Atrial é a arritmia sustentada mais comum do mundo ocidental, ocorrendo com frequência cada vez maior à medida que a população envelhece. Uma arritmia isolada ou de ocorrência familial, fibrilação atrial no passado era considerada benigna, mas com o passar dos anos e com a complexidade dos estudos médicos, verificou-se que a fibrilação atrial acompanha ou é causa de muitas morbidades.
Na fibrilação atrial ocorre uma alteração na formação do estímulo cardíaco nos átrios. Ocorre uma espécie de curto circuito em várias áreas dos átrios, gerando inúmeros diminutos estímulos simultânea. Ocasionando uma desorganização elétrica tamanha que o coração torna-se incapaz de gerar a contração dos átrios.
Como há uma filtração importante no nodo sinoatrial, acaba que apenas um estímulo prossegue para os ventrículos por vez. Entretanto, apesar da filtração eficiente há transmissões elétricas descompassadas e rápidas para os ventrículos, ou seja, o coração acaba por bater de forma irregular e acelerada.
Em vez de contraírem, os átrios fibrilam – apresentam um movimento como se fosse um tremor grosseiro. E esta movimentação anômala gera um fluxo irregular do sangue, propiciando a formação de trombos dentro das cavidades cardíacas. Uma vez formados, os trombos podem migrar para os pulmões (gerando embolia pulmonar), para o cérebro (gerando AVC) e para os órgãos periféricos (rins, fígado, intestino, etc…).
Uma observação importância é quanto a incidência, segundo a Sociedade Brasileira de Cardiologia, cerca de um em cada 10 mil jovens brasileiros sem problemas cardiopaticos aparante tem fibrilação atrial. Nesses indivíduos, a doença é geralmente intermitente, mas 25% dos casos pode se tornar uma doença crônica.
O impacto da fibrilação atrial na morbimortalidade da população é elevado, bem como suas consequências socioeconômicas, relacionado, principalmente, a internações hospitalares, manejo crônico da doença e incapacitação ou limitação física de seus portadores, neste caso, mais comumente nos idosos.
- Fatores de Risco
-
A Fibrilação Atrial é uma doença um pouco diferente das que conhecemos, pois não existe uma relação causa-consequência única!
Existem inúmeras possibilidades e elas podem estar atuando ao mesmo tempo em um mesmo indivíduo!
Podemos citar:
- álcool
- tabagismo
- apneia do sono
- doença cardíaca
- hipertensão arterial sistêmica
- diabetes
- entorpecentes
- cirurgias
- obesidade
- histórico familiar
- distúrbios metabólicos
Causas reversíveis de Fibrilação Atrial
Fibrilação Atrial pode ser provocada durante situações transitórias, incluindo a ingestão de álcool, cirurgias, choque elétrico, infarto do miocárdio, pericardite, miocardite, embolia pulmonar, outras doenças pulmonares, hipertireoidismo e outras doenças metabólicas. - Sintomas
-
Algumas vezes a fibrilação atrial não apresenta sintomas, porém quando surgem, os sintomas mais comuns são:
- Palpitações no peito
- Fraqueza/Fadiga
- Capacidade reduzida de se exercitar
- Tontura
- Confusão
- Falta de ar
- Dor no peito
- Desmaio.
- Diagnóstico
-
Como é uma arritmia comum, bons clínicos gerais e outros especialistas conseguem identificá-la facilmente, apenas através da palpação e ausculta de um ritmo cardíaco caótico. Mas a documentação através do eletrocardiograma simples, de 12 derivações, é o exame padrão, não sendo necessária nenhuma confirmação diagnóstica complementar. Então o paciente poderá ser encaminhado a um cardiologista, que assim procederá a investigação das causas, estimativa dos riscos e proposta de tratamento.
- Tratamento
-
Existem algumas opções de tratamento para a Fibrilação Atrial como: medicações, cardioversão elétrica (choque elétrico no tórax), ablação por cateter ou cirurgia.
- Estadiamento
-
Não há estadiamento.
O câncer de vulva é um câncer raro, responsável por 0,5% de todos os cânceres nas mulheres e 5% dos tumores ginecológicos. O tipo mais comum deste câncer é o carcinoma espinocelular, um câncer de pele que surge como uma mancha ou ferida que não cicatriza e vai aumentando.
O câncer de vulva aparece com mais frequente em mulheres após a menopausa, porém alguns fatores podem favorecer o surgimento da doença em idades mais jovens.
Os principais fatores de risco do câncer de vulva são:
- Idade: mulheres com mais de 50 anos, sendo a incidência maior após os 70 anos;
- Irritação/inflamação vulvar crônica;
- Infecção pelo vírus HPV (Vírus do Papiloma Humano);
- Infecção pelo vírus HIV (Vírus da Imunodeficiência Humana);
- Tabagismo;
- Neoplasia intraepitelial de Vulva (displasia vulvar): lesão pré-maligna formada por células anormais na camada mais superficial da pele da vulva;
- Outros Cânceres Genitais como câncer de colo do útero;
- Melanoma ou Pintas Atípicas.
Os sintomas mais frequentes do câncer de Vulva são:
- Ferida que não cicatriza (sintoma mais frequente);
- Ardência;
- Coceira na região;
- Mancha ou caroço (que pode se transformar em ferida ou descamar);
- Mulheres infectadas com HPV;
- Inflamação e Irritação na vagina;
- Infecção na vagina;
- Sangramento;
- Nódulo ou ulceração;
- Áreas de pele com cor e textura alteradas.
O diagnóstico do câncer de vulva é feito por histórico clínico e exame físico, confirmado por meio de biópsia. Habitualmente a biópsia da vulva é um procedimento ambulatorial, realizado pelo médico com uso de anestesia local. Outros exames utilizados no diagnóstico são: exames de imagem (Ressonância Magnética, Tomografia Computadorizada, Petscan (tomografia por emissão de pósitrons) e Radiografia de Tórax) e Cistoscopia(que examina a parte superior da bexiga), Proctoscopia (examina o reto) e exame pélvico.
Os tumores em estágio inicial são tratados por cirurgia, onde tumor e os gânglios linfáticos inguinais – primeiro local para onde o câncer da vulva pode espalhar- são removidos. Já os tumores avançados podem ser tratados com quimioterapia e radioterapia, antes ou após da cirurgia.
Os tratamentos utilizados são:
- Cirurgias;
- Terapia com laser: destruição das células anormais utilizando um feixe de luz concentrada (laser) pode ser utilizada no tratamento das lesões pré-malignas (Neoplasia Intra-Epitelial Vulvar ou NIV);
- Vulvectomia simples: ressecção de toda a vulva;
- Vulvectomia radical: remoção da vulva com tecido normal ao redor e inclui esvaziamento dos gânglios linfáticos inguinais;
- Linfadenectomia: ressecção dos gânglios linfáticos;
- Radioterapia: utiliza feixes de radiação para destruir as células tumorais.
É preciso que o médico e o paciente estejam sempre atentos ao estadiamento da doença! Mas, o que é estadiamento? São os estágios que o câncer está no momento, ou seja, o tamanho, a localização e se espalhou para outros órgãos. O estádio de um tumor reflete não apenas a taxa de crescimento e a extensão da doença, mas também o tipo de tumor e sua relação com o hospedeiro. O sistema de estadiamento mais utilizado é o TNM da American Joint Committee on Cancer.
O que é TNM?
É a abreviatura de tumor, linfonodo e metástase. Este sistema utiliza três critérios para avaliar o estágio do câncer:
- O próprio tumor ( T + um número de 0 a 4 usa-se para descrever o tumor primário);
- Os linfonodos regionais ao redor do tumor ( N + 0 a 3 usa-se para descrever se a doença disseminou para os gânglios linfáticos)
- E se o tumor se espalhou para outras partes do corpo (M usa-se para descrever que a doença se espalhou para outros órgãos)
O estadiamento pode ser clínico e patológico. O estadiamento clínico é estabelecido a partir dos dados do exame físico e dos exames complementares. O estadiamento patológico baseia-se nos achados cirúrgicos e no exame anátomopatológico – é estabelecido após tratamento cirúrgico e determina a extensão da doença com maior precisão. Lembrando que o estadiamento patológico pode ou não coincidir com o estadiamento clínico e não é aplicável a todos os tumores.
E o estadiamento para Câncer de Vulva, como funciona?
O Estadiamento da Federação Internacional de Ginecologia e Obstetrícia (FIGO) adota como critérios o tamanho do tumor, invasão das estruturas perineais, comprometimento dos linfonodos e metástases à distância:
TNM
T – Tumor primário
TTis – Carcinoma pré-invasivo
T1 – Tumor confinado à vulva e/ou períneo com 2,0 cm ou menos na sua maior dimensão
T2 – Tumor confinado à vulva e/ou períneo com mais de 2,0 cm na sua maior dimensão
T3 – Tumor de qualquer tamanho com invasão da uretra e/ou ânus
T4 – Tumor de qualquer tamanho infiltrando a mucosa vesical e/ou retal, incluindo a porção superior da mucosa uretral e/ou ânus
N – Linfonodos regionais
N0 – Linfonodos não palpáveis
N1 – Linfonodos regionais unilaterais metastáticos
N2 – Linfonodos regionais bilaterais metastáticos
M – Metástase à distância
M0 – Ausência de metástases
Estadiamento cirúrgico do câncer vulvar:
O Tis Carcinoma in situ (Carcinoma pré-invasivo)
I
T1N0M0: Tumor confinado à vulva e/ou períneo maior diâmetro menor que 2,0 cm e linfonodos inguinais negativos
T1a Invasão estromal inferior a 1,0 mm inclusive
T1b Invasão estromal superior a 1,0 mm
II
T2N0M0: Tumor confinado a vulva e/ou períneo com maior diâmetro superior a 2,0 cm e linfonodos inguinais negativos
III
T1N1M0 / T2N1M0: Tumor de qualquer tamanho infiltrando a porção inferior da uretra e/ou vagina ou ânus e/ou metástase linfonodal regional unilateral
T3N0M0 / T3N1M0
IVA
T1N2M0: Tumor invade porção superior da uretra,mucosa vesical, mucosa retal, osso pélvico e/ou linfonodos regionais bilaterais
T2N2M0 / T3N2M0 / T4NqqM0
IVBT
qqNqqM1 : Metástases à distância, incluindo linfonodos pélvicos
Fonte: Associação Médica Brasileira e Agência Nacional de Saúde Suplementar
O câncer de vulva é um câncer raro, responsável por 0,5% de todos os cânceres nas mulheres e 5% dos tumores ginecológicos. O tipo mais comum deste câncer é o carcinoma espinocelular, um câncer de pele que surge como uma mancha ou ferida que não cicatriza e vai aumentando.
O câncer de vulva aparece com mais frequente em mulheres após a menopausa, porém alguns fatores podem favorecer o surgimento da doença em idades mais jovens.
Os principais fatores de risco do câncer de vulva são:
- Idade: mulheres com mais de 50 anos, sendo a incidência maior após os 70 anos;
- Irritação/inflamação vulvar crônica;
- Infecção pelo vírus HPV (Vírus do Papiloma Humano);
- Infecção pelo vírus HIV (Vírus da Imunodeficiência Humana);
- Tabagismo;
- Neoplasia intraepitelial de Vulva (displasia vulvar): lesão pré-maligna formada por células anormais na camada mais superficial da pele da vulva;
- Outros Cânceres Genitais como câncer de colo do útero;
- Melanoma ou Pintas Atípicas.
Os sintomas mais frequentes do câncer de Vulva são:
- Ferida que não cicatriza (sintoma mais frequente);
- Ardência;
- Coceira na região;
- Mancha ou caroço (que pode se transformar em ferida ou descamar);
- Mulheres infectadas com HPV;
- Inflamação e Irritação na vagina;
- Infecção na vagina;
- Sangramento;
- Nódulo ou ulceração;
- Áreas de pele com cor e textura alteradas.
O diagnóstico do câncer de vulva é feito por histórico clínico e exame físico, confirmado por meio de biópsia. Habitualmente a biópsia da vulva é um procedimento ambulatorial, realizado pelo médico com uso de anestesia local. Outros exames utilizados no diagnóstico são: exames de imagem (Ressonância Magnética, Tomografia Computadorizada, Petscan (tomografia por emissão de pósitrons) e Radiografia de Tórax) e Cistoscopia(que examina a parte superior da bexiga), Proctoscopia (examina o reto) e exame pélvico.
Os tumores em estágio inicial são tratados por cirurgia, onde tumor e os gânglios linfáticos inguinais – primeiro local para onde o câncer da vulva pode espalhar- são removidos. Já os tumores avançados podem ser tratados com quimioterapia e radioterapia, antes ou após da cirurgia.
Os tratamentos utilizados são:
- Cirurgias;
- Terapia com laser: destruição das células anormais utilizando um feixe de luz concentrada (laser) pode ser utilizada no tratamento das lesões pré-malignas (Neoplasia Intra-Epitelial Vulvar ou NIV);
- Vulvectomia simples: ressecção de toda a vulva;
- Vulvectomia radical: remoção da vulva com tecido normal ao redor e inclui esvaziamento dos gânglios linfáticos inguinais;
- Linfadenectomia: ressecção dos gânglios linfáticos;
- Radioterapia: utiliza feixes de radiação para destruir as células tumorais.
É preciso que o médico e o paciente estejam sempre atentos ao estadiamento da doença! Mas, o que é estadiamento? São os estágios que o câncer está no momento, ou seja, o tamanho, a localização e se espalhou para outros órgãos. O estádio de um tumor reflete não apenas a taxa de crescimento e a extensão da doença, mas também o tipo de tumor e sua relação com o hospedeiro. O sistema de estadiamento mais utilizado é o TNM da American Joint Committee on Cancer.
O que é TNM?
É a abreviatura de tumor, linfonodo e metástase. Este sistema utiliza três critérios para avaliar o estágio do câncer:
- O próprio tumor ( T + um número de 0 a 4 usa-se para descrever o tumor primário);
- Os linfonodos regionais ao redor do tumor ( N + 0 a 3 usa-se para descrever se a doença disseminou para os gânglios linfáticos)
- E se o tumor se espalhou para outras partes do corpo (M usa-se para descrever que a doença se espalhou para outros órgãos)
O estadiamento pode ser clínico e patológico. O estadiamento clínico é estabelecido a partir dos dados do exame físico e dos exames complementares. O estadiamento patológico baseia-se nos achados cirúrgicos e no exame anátomopatológico – é estabelecido após tratamento cirúrgico e determina a extensão da doença com maior precisão. Lembrando que o estadiamento patológico pode ou não coincidir com o estadiamento clínico e não é aplicável a todos os tumores.
E o estadiamento para Câncer de Vulva, como funciona?
O Estadiamento da Federação Internacional de Ginecologia e Obstetrícia (FIGO) adota como critérios o tamanho do tumor, invasão das estruturas perineais, comprometimento dos linfonodos e metástases à distância:
TNM
T – Tumor primário
TTis – Carcinoma pré-invasivo
T1 – Tumor confinado à vulva e/ou períneo com 2,0 cm ou menos na sua maior dimensão
T2 – Tumor confinado à vulva e/ou períneo com mais de 2,0 cm na sua maior dimensão
T3 – Tumor de qualquer tamanho com invasão da uretra e/ou ânus
T4 – Tumor de qualquer tamanho infiltrando a mucosa vesical e/ou retal, incluindo a porção superior da mucosa uretral e/ou ânus
N – Linfonodos regionais
N0 – Linfonodos não palpáveis
N1 – Linfonodos regionais unilaterais metastáticos
N2 – Linfonodos regionais bilaterais metastáticos
M – Metástase à distância
M0 – Ausência de metástases
Estadiamento cirúrgico do câncer vulvar:
O Tis Carcinoma in situ (Carcinoma pré-invasivo)
I
T1N0M0: Tumor confinado à vulva e/ou períneo maior diâmetro menor que 2,0 cm e linfonodos inguinais negativos
T1a Invasão estromal inferior a 1,0 mm inclusive
T1b Invasão estromal superior a 1,0 mm
II
T2N0M0: Tumor confinado a vulva e/ou períneo com maior diâmetro superior a 2,0 cm e linfonodos inguinais negativos
III
T1N1M0 / T2N1M0: Tumor de qualquer tamanho infiltrando a porção inferior da uretra e/ou vagina ou ânus e/ou metástase linfonodal regional unilateral
T3N0M0 / T3N1M0
IVA
T1N2M0: Tumor invade porção superior da uretra,mucosa vesical, mucosa retal, osso pélvico e/ou linfonodos regionais bilaterais
T2N2M0 / T3N2M0 / T4NqqM0
IVBT
qqNqqM1 : Metástases à distância, incluindo linfonodos pélvicos
Fonte: Associação Médica Brasileira e Agência Nacional de Saúde Suplementar
- O que é?
-
O câncer de vulva é um câncer raro, responsável por 0,5% de todos os cânceres nas mulheres e 5% dos tumores ginecológicos. O tipo mais comum deste câncer é o carcinoma espinocelular, um câncer de pele que surge como uma mancha ou ferida que não cicatriza e vai aumentando.
O câncer de vulva aparece com mais frequente em mulheres após a menopausa, porém alguns fatores podem favorecer o surgimento da doença em idades mais jovens. - Fatores de Risco
-
Os principais fatores de risco do câncer de vulva são:
- Idade: mulheres com mais de 50 anos, sendo a incidência maior após os 70 anos;
- Irritação/inflamação vulvar crônica;
- Infecção pelo vírus HPV (Vírus do Papiloma Humano);
- Infecção pelo vírus HIV (Vírus da Imunodeficiência Humana);
- Tabagismo;
- Neoplasia intraepitelial de Vulva (displasia vulvar): lesão pré-maligna formada por células anormais na camada mais superficial da pele da vulva;
- Outros Cânceres Genitais como câncer de colo do útero;
- Melanoma ou Pintas Atípicas.
- Sintomas
-
Os sintomas mais frequentes do câncer de Vulva são:
- Ferida que não cicatriza (sintoma mais frequente);
- Ardência;
- Coceira na região;
- Mancha ou caroço (que pode se transformar em ferida ou descamar);
- Mulheres infectadas com HPV;
- Inflamação e Irritação na vagina;
- Infecção na vagina;
- Sangramento;
- Nódulo ou ulceração;
- Áreas de pele com cor e textura alteradas.
- Diagnóstico
-
O diagnóstico do câncer de vulva é feito por histórico clínico e exame físico, confirmado por meio de biópsia. Habitualmente a biópsia da vulva é um procedimento ambulatorial, realizado pelo médico com uso de anestesia local. Outros exames utilizados no diagnóstico são: exames de imagem (Ressonância Magnética, Tomografia Computadorizada, Petscan (tomografia por emissão de pósitrons) e Radiografia de Tórax) e Cistoscopia(que examina a parte superior da bexiga), Proctoscopia (examina o reto) e exame pélvico.
- Tratamento
-
Os tumores em estágio inicial são tratados por cirurgia, onde tumor e os gânglios linfáticos inguinais – primeiro local para onde o câncer da vulva pode espalhar- são removidos. Já os tumores avançados podem ser tratados com quimioterapia e radioterapia, antes ou após da cirurgia.
Os tratamentos utilizados são:
- Cirurgias;
- Terapia com laser: destruição das células anormais utilizando um feixe de luz concentrada (laser) pode ser utilizada no tratamento das lesões pré-malignas (Neoplasia Intra-Epitelial Vulvar ou NIV);
- Vulvectomia simples: ressecção de toda a vulva;
- Vulvectomia radical: remoção da vulva com tecido normal ao redor e inclui esvaziamento dos gânglios linfáticos inguinais;
- Linfadenectomia: ressecção dos gânglios linfáticos;
- Radioterapia: utiliza feixes de radiação para destruir as células tumorais.
- Estadiamento
-
É preciso que o médico e o paciente estejam sempre atentos ao estadiamento da doença! Mas, o que é estadiamento? São os estágios que o câncer está no momento, ou seja, o tamanho, a localização e se espalhou para outros órgãos. O estádio de um tumor reflete não apenas a taxa de crescimento e a extensão da doença, mas também o tipo de tumor e sua relação com o hospedeiro. O sistema de estadiamento mais utilizado é o TNM da American Joint Committee on Cancer.
O que é TNM?
É a abreviatura de tumor, linfonodo e metástase. Este sistema utiliza três critérios para avaliar o estágio do câncer:
- O próprio tumor ( T + um número de 0 a 4 usa-se para descrever o tumor primário);
- Os linfonodos regionais ao redor do tumor ( N + 0 a 3 usa-se para descrever se a doença disseminou para os gânglios linfáticos)
- E se o tumor se espalhou para outras partes do corpo (M usa-se para descrever que a doença se espalhou para outros órgãos)
O estadiamento pode ser clínico e patológico. O estadiamento clínico é estabelecido a partir dos dados do exame físico e dos exames complementares. O estadiamento patológico baseia-se nos achados cirúrgicos e no exame anátomopatológico – é estabelecido após tratamento cirúrgico e determina a extensão da doença com maior precisão. Lembrando que o estadiamento patológico pode ou não coincidir com o estadiamento clínico e não é aplicável a todos os tumores.
E o estadiamento para Câncer de Vulva, como funciona?
O Estadiamento da Federação Internacional de Ginecologia e Obstetrícia (FIGO) adota como critérios o tamanho do tumor, invasão das estruturas perineais, comprometimento dos linfonodos e metástases à distância:
TNM
T – Tumor primário
TTis – Carcinoma pré-invasivo
T1 – Tumor confinado à vulva e/ou períneo com 2,0 cm ou menos na sua maior dimensão
T2 – Tumor confinado à vulva e/ou períneo com mais de 2,0 cm na sua maior dimensão
T3 – Tumor de qualquer tamanho com invasão da uretra e/ou ânus
T4 – Tumor de qualquer tamanho infiltrando a mucosa vesical e/ou retal, incluindo a porção superior da mucosa uretral e/ou ânus
N – Linfonodos regionais
N0 – Linfonodos não palpáveis
N1 – Linfonodos regionais unilaterais metastáticos
N2 – Linfonodos regionais bilaterais metastáticos
M – Metástase à distância
M0 – Ausência de metástases
Estadiamento cirúrgico do câncer vulvar:
O Tis Carcinoma in situ (Carcinoma pré-invasivo)
I
T1N0M0: Tumor confinado à vulva e/ou períneo maior diâmetro menor que 2,0 cm e linfonodos inguinais negativos
T1a Invasão estromal inferior a 1,0 mm inclusive
T1b Invasão estromal superior a 1,0 mm
II
T2N0M0: Tumor confinado a vulva e/ou períneo com maior diâmetro superior a 2,0 cm e linfonodos inguinais negativos
III
T1N1M0 / T2N1M0: Tumor de qualquer tamanho infiltrando a porção inferior da uretra e/ou vagina ou ânus e/ou metástase linfonodal regional unilateral
T3N0M0 / T3N1M0
IVA
T1N2M0: Tumor invade porção superior da uretra,mucosa vesical, mucosa retal, osso pélvico e/ou linfonodos regionais bilaterais
T2N2M0 / T3N2M0 / T4NqqM0
IVBT
qqNqqM1 : Metástases à distância, incluindo linfonodos pélvicos
Fonte: Associação Médica Brasileira e Agência Nacional de Saúde Suplementar
O Câncer de Colo de Útero é um tumor que ataca a área inferior do útero, chamada de colo ou cérvix. Os primeiros sintomas são verrugas na mucosa da vagina, do pênis, do ânus, da laringe e do esôfago. Esta é uma doença que demora anos para desenvolver, aproximadamente, de 10 a 20 anos.
Este é o segundo tipo de câncer feminino mais comum, perdendo apenas para o câncer de mama.Segundo o Instituto Nacional do Câncer – INCA, no Brasil, está em terceiro lugar, atrás do câncer de mama e intestino (colon e reto), com taxa de incidência de 15 novos casos em 100.000 mulheres ao ano. A mortalidade pode chegar a 5 casos em 100.000 ao ano. Geralmente, afeta mulheres entre 40 e 60 anos de idade.
A endometriose (outra doença muito comum as mulheres adultas) e a genética não possuem relação com o surgimento desse câncer. O Câncer de Colo de Útero pode evoluir para uma doença mais severa, o Carcinoma invasor do colo uterino (tumor maligno).
Alguns riscos possibilitam o aparecimento do Câncer de Colo do Útero:
- Sexo desprotegido com múltiplos parceiros
- Histórico de DSTs (HPV – Papiloma Vírus Humano)
- Tabagismo
- Idade precoce da primeira relação sexual
- Má higiene íntima
- Multiparidade (Várias gravidezes)
Por ser uma doença lenta, na maioria dos casos, quando os sintomas aparecem é sinal de que o câncer está em estágio avançado.
Os sintomas variam conforme a gravidade da doença:
- Corrimento persistente de coloração amarelada ou rosa e com forte odor;
- Hemorragia anormal;
- Desconforto ao urinar;
- Micção irregular;
- Ciclos menstruais irregulares;
- Sexo desconfortável (com dor);
- Dor na pelve;
- Dor nas costas;
O principal exame para prevenir e detectar o Câncer do colo de útero é o Papanicolau. Este exame faz parte dos exames de rotina da saúde da mulher e permite ao médico examinar visualmente o interior da vagina e o colo do útero. Com uma espátula de madeira e uma pequena escova especial o médico realiza a descamação do colo do útero a fim de recolher as células para a análise em laboratório. O Papanicolau pode ser complementado com Colposcopia com a realização de biópsia para se confirmar o diagnóstico.
Os tratamentos aplicados para o Câncer de colo do útero podem ser:
Cirurgia – Este procedimento consiste na retirada do tumor e, em algum casos, do útero e da parte superior da vagina também.
Radioterapia – O objetivo deste tratamento é reduzir o volume volume tumoral.
Quimioterapia – Este tratamento é indicado para tumores em estágios mais avançados.
O tipo de tratamento irá depender do estágio da doença, do tamanho do tumor e fatores pessoais, como idade e desejo de ter filhos.
Em atualização.
Mais informações acesse o site da International Myeloma Foundation Latin America – IMF Latin America ou ligue para ligue para 0800 777 0355 (IMF Latin America) e saiba tudo sobre essa doença!
O Câncer de Colo de Útero é um tumor que ataca a área inferior do útero, chamada de colo ou cérvix. Os primeiros sintomas são verrugas na mucosa da vagina, do pênis, do ânus, da laringe e do esôfago. Esta é uma doença que demora anos para desenvolver, aproximadamente, de 10 a 20 anos.
Este é o segundo tipo de câncer feminino mais comum, perdendo apenas para o câncer de mama.Segundo o Instituto Nacional do Câncer – INCA, no Brasil, está em terceiro lugar, atrás do câncer de mama e intestino (colon e reto), com taxa de incidência de 15 novos casos em 100.000 mulheres ao ano. A mortalidade pode chegar a 5 casos em 100.000 ao ano. Geralmente, afeta mulheres entre 40 e 60 anos de idade.
A endometriose (outra doença muito comum as mulheres adultas) e a genética não possuem relação com o surgimento desse câncer. O Câncer de Colo de Útero pode evoluir para uma doença mais severa, o Carcinoma invasor do colo uterino (tumor maligno).
Alguns riscos possibilitam o aparecimento do Câncer de Colo do Útero:
- Sexo desprotegido com múltiplos parceiros
- Histórico de DSTs (HPV – Papiloma Vírus Humano)
- Tabagismo
- Idade precoce da primeira relação sexual
- Má higiene íntima
- Multiparidade (Várias gravidezes)
Por ser uma doença lenta, na maioria dos casos, quando os sintomas aparecem é sinal de que o câncer está em estágio avançado.
Os sintomas variam conforme a gravidade da doença:
- Corrimento persistente de coloração amarelada ou rosa e com forte odor;
- Hemorragia anormal;
- Desconforto ao urinar;
- Micção irregular;
- Ciclos menstruais irregulares;
- Sexo desconfortável (com dor);
- Dor na pelve;
- Dor nas costas;
O principal exame para prevenir e detectar o Câncer do colo de útero é o Papanicolau. Este exame faz parte dos exames de rotina da saúde da mulher e permite ao médico examinar visualmente o interior da vagina e o colo do útero. Com uma espátula de madeira e uma pequena escova especial o médico realiza a descamação do colo do útero a fim de recolher as células para a análise em laboratório. O Papanicolau pode ser complementado com Colposcopia com a realização de biópsia para se confirmar o diagnóstico.
Os tratamentos aplicados para o Câncer de colo do útero podem ser:
Cirurgia – Este procedimento consiste na retirada do tumor e, em algum casos, do útero e da parte superior da vagina também.
Radioterapia – O objetivo deste tratamento é reduzir o volume volume tumoral.
Quimioterapia – Este tratamento é indicado para tumores em estágios mais avançados.
O tipo de tratamento irá depender do estágio da doença, do tamanho do tumor e fatores pessoais, como idade e desejo de ter filhos.
Em atualização.
- O que é?
-
O Câncer de Colo de Útero é um tumor que ataca a área inferior do útero, chamada de colo ou cérvix. Os primeiros sintomas são verrugas na mucosa da vagina, do pênis, do ânus, da laringe e do esôfago. Esta é uma doença que demora anos para desenvolver, aproximadamente, de 10 a 20 anos.
Este é o segundo tipo de câncer feminino mais comum, perdendo apenas para o câncer de mama.Segundo o Instituto Nacional do Câncer – INCA, no Brasil, está em terceiro lugar, atrás do câncer de mama e intestino (colon e reto), com taxa de incidência de 15 novos casos em 100.000 mulheres ao ano. A mortalidade pode chegar a 5 casos em 100.000 ao ano. Geralmente, afeta mulheres entre 40 e 60 anos de idade.
A endometriose (outra doença muito comum as mulheres adultas) e a genética não possuem relação com o surgimento desse câncer. O Câncer de Colo de Útero pode evoluir para uma doença mais severa, o Carcinoma invasor do colo uterino (tumor maligno).
- Fatores de Risco
-
Alguns riscos possibilitam o aparecimento do Câncer de Colo do Útero:
- Sexo desprotegido com múltiplos parceiros
- Histórico de DSTs (HPV – Papiloma Vírus Humano)
- Tabagismo
- Idade precoce da primeira relação sexual
- Má higiene íntima
- Multiparidade (Várias gravidezes)
- Sintomas
-
Por ser uma doença lenta, na maioria dos casos, quando os sintomas aparecem é sinal de que o câncer está em estágio avançado.
Os sintomas variam conforme a gravidade da doença:
- Corrimento persistente de coloração amarelada ou rosa e com forte odor;
- Hemorragia anormal;
- Desconforto ao urinar;
- Micção irregular;
- Ciclos menstruais irregulares;
- Sexo desconfortável (com dor);
- Dor na pelve;
- Dor nas costas;
- Diagnóstico
-
O principal exame para prevenir e detectar o Câncer do colo de útero é o Papanicolau. Este exame faz parte dos exames de rotina da saúde da mulher e permite ao médico examinar visualmente o interior da vagina e o colo do útero. Com uma espátula de madeira e uma pequena escova especial o médico realiza a descamação do colo do útero a fim de recolher as células para a análise em laboratório. O Papanicolau pode ser complementado com Colposcopia com a realização de biópsia para se confirmar o diagnóstico.
- Tratamento
-
Os tratamentos aplicados para o Câncer de colo do útero podem ser:
Cirurgia – Este procedimento consiste na retirada do tumor e, em algum casos, do útero e da parte superior da vagina também.
Radioterapia – O objetivo deste tratamento é reduzir o volume volume tumoral.
Quimioterapia – Este tratamento é indicado para tumores em estágios mais avançados.
O tipo de tratamento irá depender do estágio da doença, do tamanho do tumor e fatores pessoais, como idade e desejo de ter filhos.
- Estadiamento
-
Em atualização.
A leucemia é um câncer das primeiras células formadoras de sangue. Na maioria das vezes, a leucemia é um câncer dos glóbulos brancos do sangue, mas algumas leucemias começam em outros tipos de células do sangue. Existem vários tipos de leucemias, que são divididas principalmente com base em se a leucemia é aguda (crescimento rápido) ou crônica (crescimento mais lento) e se começa nas células mielóides ou células linfóides. Diferentes tipos de leucemia têm diferentes opções de tratamento e perspectivas.
Quais são os tipos de Leucemia?
Leucemia Linfoide Aguda (LLA)
A leucemia linfocide aguda (ou linfoblástica) às vezes é chamada de LLA. Começa na medula óssea, onde são feitas as células sanguíneas. É mais comum em crianças do que em adultos.
Leucemia Mieloide Aguda (LMA) em Adultos
A leucemia mieloide aguda (LMA) começa na medula óssea (a parte interna mole de certos ossos, onde novas células sanguíneas são feitas – as células-tronco). Às vezes, pode se espalhar para outras partes do corpo, incluindo os gânglios linfáticos, fígado, baço, sistema nervoso central (cérebro e medula espinhal) e testículos. A LMA se desenvolve a partir de células que se transformariam em glóbulos brancos (exceto linfócitos), mas às vezes a LMA se desenvolve em outros tipos de células formadoras de sangue. A leucemia mieloide aguda (LMA) tem muitos outros nomes, incluindo leucemia mielocítica aguda, leucemia mieloide aguda, leucemia granulocítica aguda e leucemia não linfocítica aguda.
Leucemia Linfoide Crônica (LLC)
É a leucemia mais comum em adultos. É um tipo de câncer que começa nas células que se transformam em certos glóbulos brancos (chamados linfócitos) na medula óssea. As células cancerosas (leucemia) começam na medula óssea, mas depois vão para o sangue. Na LLC, as células leucêmicas frequentemente se acumulam lentamente. Muitas pessoas não apresentam sintomas por pelo menos alguns anos. Mas, com o tempo, as células crescem e se espalham para outras partes do corpo, incluindo os gânglios linfáticos, fígado e baço.
Leucemia Mieloide Crônica (LMC)
Também conhecida como leucemia mielogênica crônica
É um tipo de câncer que começa em certas células formadoras de sangue da medula óssea. Na LMC, uma mudança genética ocorre em uma versão inicial (imatura) das células mieloides – as células que produzem glóbulos vermelhos, plaquetas e a maioria dos tipos de glóbulos brancos (exceto linfócitos). Essa mudança forma um gene anormal chamado BCR-ABL, que transforma a célula em uma célula LMC. As células leucêmicas crescem e se dividem, acumulando-se na medula óssea e transbordando para o sangue. Com o tempo, as células também podem se estabelecer em outras partes do corpo, incluindo o baço. LMC é uma leucemia de crescimento bastante lento, mas pode se transformar em uma leucemia aguda de crescimento rápido que é difícil de tratar. A LMC ocorre principalmente em adultos, mas muito raramente também ocorre em crianças. Em geral, o tratamento é igual ao dos adultos.
Leucemia Mielomonocítica Crônica (LMMC)
Começa nas células formadoras de sangue na medula óssea e invade o sangue. As células em quase qualquer parte do corpo podem se tornar câncer e podem se espalhar para outras áreas do corpo. Pessoas com LMMC podem ter falta de algumas células sanguíneas, mas o principal problema são os monócitos em excesso, um tipo de glóbulos brancos. (pelo menos 1.000 por mm3). Frequentemente, a contagem de monócitos é muito maior, fazendo com que sua contagem total de leucócitos também fique muito alta.Normalmente, existem algumas células anormais, chamadas blastos, na medula óssea. A quantidade de explosões na LMMC é inferior a 20%.Muitas pessoas com LMMC têm baços aumentados (um órgão que fica logo abaixo da caixa torácica esquerda).Cerca de 15% a 30% das pessoas com LMMC desenvolvem leucemia mieloide aguda (LMA)O DNA dentro das células anormais não tem certas mudanças nos genes chamados BCR / ABL (cromossomo Filadélfia), ou PDGFRA e PDGRFRB. Como a LMMC tem características tanto de síndrome mielodisplásica quanto de neoplasia mieloproliferativa, os especialistas criaram uma nova categoria para ela: neoplasia mielodisplásica / mieloproliferativa (mielo – medula óssea, proliferativa – crescimento excessivo, displásica – aparência anormal). A LMMC é a doença mais comum nesse grupo. Doenças muito menos comuns nesse grupo são a leucemia mieloide crônica atípica e a leucemia mielomonocítica juvenil (LMMJ). Todas essas doenças produzem muitas células sanguíneas anormais. A leucemia mieloide crônica é um exemplo de neoplasia mieloproliferativa em que há uma superprodução de glóbulos brancos do sangue.
Leucemia Infantojuvenil
As leucemias são cânceres que começam nas células que normalmente se desenvolveriam em diferentes tipos de células do sangue. Na maioria das vezes, a leucemia começa nas formas iniciais de glóbulos brancos, mas algumas leucemias começam em outros tipos de células sanguíneas. Existem diferentes tipos de leucemia, que se baseiam principalmente em:
Se a leucemia for aguda (crescimento rápido) ou crônica (crescimento mais lento).
Se a leucemia começar nas células mieloides ou linfoides.
Saber o tipo específico de leucemia que uma criança e/ou adolescente tem pode ajudar os médicos a prever melhor o prognóstico (perspectiva) de cada criança e selecionar o melhor tratamento.
Leucemias Agudas
A maioria das leucemias infantojuvenis são agudas. Essas leucemias podem progredir rapidamente e geralmente precisam ser tratadas imediatamente. Os principais tipos de leucemia aguda são:
Leucemia linfocítica (linfoblástica) aguda (LLA): cerca de 3 em cada 4 leucemias infantojuvenis são LLA. Essas leucemias começam nas primeiras formas de glóbulos brancos do sangue chamadas linfócitos.
Leucemia mieloide aguda (LMA): este tipo de leucemia, também chamada de ou leucemia não linfocítica aguda, é responsável pela maioria dos casos restantes de leucemia infantojuvenil. A LMA começa a partir das células mieloides que normalmente formam os glóbulos brancos (exceto linfócitos), glóbulos vermelhos ou plaquetas.
Raramente, as leucemias agudas podem apresentar características tanto de LLA quanto de LMA. Estas são chamadas de leucemias de linhagem mista, leucemias agudas indiferenciadas ou Leucemias Agudas de Fenótipo Misto.
Leucemia Crônica
As leucemias crônicas são raras em crianças e adolescentes. Essas leucemias tendem a crescer mais lentamente do que as leucemias agudas, mas também são mais difíceis de curar. As leucemias crônicas podem ser divididas em 2 tipos principais:
Leucemia mieloide crônica (LMC): também chamada de leucemia mieloide crônica, a LMA é rara em crianças e adolescentes. O tratamento é semelhante ao usado para adultos.
Leucemia linfocítica crônica (LLC): essa leucemia é extremamente rara em crianças e adolescentes.
Leucemia Mielomonocítica Juvenil (LMMJ)
Este tipo raro de leucemia não é crônica nem aguda. Começa nas células mieloides, mas geralmente não cresce tão rápido quanto a LMA ou tão lentamente quanto a LMC. Ocorre com mais frequência em crianças pequenas (idade média de 2 anos). Os sintomas podem incluir pele pálida, febre, tosse, hematomas ou sangramento fácil, dificuldade para respirar (devido a muitos glóbulos brancos nos pulmões), erupção cutânea e aumento do tamanho do baço, fígado e nódulos linfáticos.
Imagem: National Cancer Institute
Mais informações em breve.
Mais informações em breve.
Mais informações em breve.
Mais informações em breve.
Mais informações em breve.
Mais informações acesse o site da International Myeloma Foundation Latin America – IMF Latin America ou ligue para ligue para 0800 777 0355 (IMF Latin America) e saiba tudo sobre essa doença!
A leucemia é um câncer das primeiras células formadoras de sangue. Na maioria das vezes, a leucemia é um câncer dos glóbulos brancos do sangue, mas algumas leucemias começam em outros tipos de células do sangue. Existem vários tipos de leucemias, que são divididas principalmente com base em se a leucemia é aguda (crescimento rápido) ou crônica (crescimento mais lento) e se começa nas células mielóides ou células linfóides. Diferentes tipos de leucemia têm diferentes opções de tratamento e perspectivas.
Quais são os tipos de Leucemia?
Leucemia Linfoide Aguda (LLA)
A leucemia linfocide aguda (ou linfoblástica) às vezes é chamada de LLA. Começa na medula óssea, onde são feitas as células sanguíneas. É mais comum em crianças do que em adultos.
Leucemia Mieloide Aguda (LMA) em Adultos
A leucemia mieloide aguda (LMA) começa na medula óssea (a parte interna mole de certos ossos, onde novas células sanguíneas são feitas – as células-tronco). Às vezes, pode se espalhar para outras partes do corpo, incluindo os gânglios linfáticos, fígado, baço, sistema nervoso central (cérebro e medula espinhal) e testículos. A LMA se desenvolve a partir de células que se transformariam em glóbulos brancos (exceto linfócitos), mas às vezes a LMA se desenvolve em outros tipos de células formadoras de sangue. A leucemia mieloide aguda (LMA) tem muitos outros nomes, incluindo leucemia mielocítica aguda, leucemia mieloide aguda, leucemia granulocítica aguda e leucemia não linfocítica aguda.
Leucemia Linfoide Crônica (LLC)
É a leucemia mais comum em adultos. É um tipo de câncer que começa nas células que se transformam em certos glóbulos brancos (chamados linfócitos) na medula óssea. As células cancerosas (leucemia) começam na medula óssea, mas depois vão para o sangue. Na LLC, as células leucêmicas frequentemente se acumulam lentamente. Muitas pessoas não apresentam sintomas por pelo menos alguns anos. Mas, com o tempo, as células crescem e se espalham para outras partes do corpo, incluindo os gânglios linfáticos, fígado e baço.
Leucemia Mieloide Crônica (LMC)
Também conhecida como leucemia mielogênica crônica
É um tipo de câncer que começa em certas células formadoras de sangue da medula óssea. Na LMC, uma mudança genética ocorre em uma versão inicial (imatura) das células mieloides – as células que produzem glóbulos vermelhos, plaquetas e a maioria dos tipos de glóbulos brancos (exceto linfócitos). Essa mudança forma um gene anormal chamado BCR-ABL, que transforma a célula em uma célula LMC. As células leucêmicas crescem e se dividem, acumulando-se na medula óssea e transbordando para o sangue. Com o tempo, as células também podem se estabelecer em outras partes do corpo, incluindo o baço. LMC é uma leucemia de crescimento bastante lento, mas pode se transformar em uma leucemia aguda de crescimento rápido que é difícil de tratar. A LMC ocorre principalmente em adultos, mas muito raramente também ocorre em crianças. Em geral, o tratamento é igual ao dos adultos.
Leucemia Mielomonocítica Crônica (LMMC)
Começa nas células formadoras de sangue na medula óssea e invade o sangue. As células em quase qualquer parte do corpo podem se tornar câncer e podem se espalhar para outras áreas do corpo. Pessoas com LMMC podem ter falta de algumas células sanguíneas, mas o principal problema são os monócitos em excesso, um tipo de glóbulos brancos. (pelo menos 1.000 por mm3). Frequentemente, a contagem de monócitos é muito maior, fazendo com que sua contagem total de leucócitos também fique muito alta.Normalmente, existem algumas células anormais, chamadas blastos, na medula óssea. A quantidade de explosões na LMMC é inferior a 20%.Muitas pessoas com LMMC têm baços aumentados (um órgão que fica logo abaixo da caixa torácica esquerda).Cerca de 15% a 30% das pessoas com LMMC desenvolvem leucemia mieloide aguda (LMA)O DNA dentro das células anormais não tem certas mudanças nos genes chamados BCR / ABL (cromossomo Filadélfia), ou PDGFRA e PDGRFRB. Como a LMMC tem características tanto de síndrome mielodisplásica quanto de neoplasia mieloproliferativa, os especialistas criaram uma nova categoria para ela: neoplasia mielodisplásica / mieloproliferativa (mielo – medula óssea, proliferativa – crescimento excessivo, displásica – aparência anormal). A LMMC é a doença mais comum nesse grupo. Doenças muito menos comuns nesse grupo são a leucemia mieloide crônica atípica e a leucemia mielomonocítica juvenil (LMMJ). Todas essas doenças produzem muitas células sanguíneas anormais. A leucemia mieloide crônica é um exemplo de neoplasia mieloproliferativa em que há uma superprodução de glóbulos brancos do sangue.
Leucemia Infantojuvenil
As leucemias são cânceres que começam nas células que normalmente se desenvolveriam em diferentes tipos de células do sangue. Na maioria das vezes, a leucemia começa nas formas iniciais de glóbulos brancos, mas algumas leucemias começam em outros tipos de células sanguíneas. Existem diferentes tipos de leucemia, que se baseiam principalmente em:
Se a leucemia for aguda (crescimento rápido) ou crônica (crescimento mais lento).
Se a leucemia começar nas células mieloides ou linfoides.
Saber o tipo específico de leucemia que uma criança e/ou adolescente tem pode ajudar os médicos a prever melhor o prognóstico (perspectiva) de cada criança e selecionar o melhor tratamento.
Leucemias Agudas
A maioria das leucemias infantojuvenis são agudas. Essas leucemias podem progredir rapidamente e geralmente precisam ser tratadas imediatamente. Os principais tipos de leucemia aguda são:
Leucemia linfocítica (linfoblástica) aguda (LLA): cerca de 3 em cada 4 leucemias infantojuvenis são LLA. Essas leucemias começam nas primeiras formas de glóbulos brancos do sangue chamadas linfócitos.
Leucemia mieloide aguda (LMA): este tipo de leucemia, também chamada de ou leucemia não linfocítica aguda, é responsável pela maioria dos casos restantes de leucemia infantojuvenil. A LMA começa a partir das células mieloides que normalmente formam os glóbulos brancos (exceto linfócitos), glóbulos vermelhos ou plaquetas.
Raramente, as leucemias agudas podem apresentar características tanto de LLA quanto de LMA. Estas são chamadas de leucemias de linhagem mista, leucemias agudas indiferenciadas ou Leucemias Agudas de Fenótipo Misto.
Leucemia Crônica
As leucemias crônicas são raras em crianças e adolescentes. Essas leucemias tendem a crescer mais lentamente do que as leucemias agudas, mas também são mais difíceis de curar. As leucemias crônicas podem ser divididas em 2 tipos principais:
Leucemia mieloide crônica (LMC): também chamada de leucemia mieloide crônica, a LMA é rara em crianças e adolescentes. O tratamento é semelhante ao usado para adultos.
Leucemia linfocítica crônica (LLC): essa leucemia é extremamente rara em crianças e adolescentes.
Leucemia Mielomonocítica Juvenil (LMMJ)
Este tipo raro de leucemia não é crônica nem aguda. Começa nas células mieloides, mas geralmente não cresce tão rápido quanto a LMA ou tão lentamente quanto a LMC. Ocorre com mais frequência em crianças pequenas (idade média de 2 anos). Os sintomas podem incluir pele pálida, febre, tosse, hematomas ou sangramento fácil, dificuldade para respirar (devido a muitos glóbulos brancos nos pulmões), erupção cutânea e aumento do tamanho do baço, fígado e nódulos linfáticos.
Imagem: National Cancer Institute
Mais informações em breve.
Mais informações em breve.
Mais informações em breve.
Mais informações em breve.
Mais informações em breve.
- O que é?
-
A leucemia é um câncer das primeiras células formadoras de sangue. Na maioria das vezes, a leucemia é um câncer dos glóbulos brancos do sangue, mas algumas leucemias começam em outros tipos de células do sangue. Existem vários tipos de leucemias, que são divididas principalmente com base em se a leucemia é aguda (crescimento rápido) ou crônica (crescimento mais lento) e se começa nas células mielóides ou células linfóides. Diferentes tipos de leucemia têm diferentes opções de tratamento e perspectivas.
Quais são os tipos de Leucemia?
Leucemia Linfoide Aguda (LLA)
A leucemia linfocide aguda (ou linfoblástica) às vezes é chamada de LLA. Começa na medula óssea, onde são feitas as células sanguíneas. É mais comum em crianças do que em adultos.
Leucemia Mieloide Aguda (LMA) em Adultos
A leucemia mieloide aguda (LMA) começa na medula óssea (a parte interna mole de certos ossos, onde novas células sanguíneas são feitas – as células-tronco). Às vezes, pode se espalhar para outras partes do corpo, incluindo os gânglios linfáticos, fígado, baço, sistema nervoso central (cérebro e medula espinhal) e testículos. A LMA se desenvolve a partir de células que se transformariam em glóbulos brancos (exceto linfócitos), mas às vezes a LMA se desenvolve em outros tipos de células formadoras de sangue. A leucemia mieloide aguda (LMA) tem muitos outros nomes, incluindo leucemia mielocítica aguda, leucemia mieloide aguda, leucemia granulocítica aguda e leucemia não linfocítica aguda.
Leucemia Linfoide Crônica (LLC)
É a leucemia mais comum em adultos. É um tipo de câncer que começa nas células que se transformam em certos glóbulos brancos (chamados linfócitos) na medula óssea. As células cancerosas (leucemia) começam na medula óssea, mas depois vão para o sangue. Na LLC, as células leucêmicas frequentemente se acumulam lentamente. Muitas pessoas não apresentam sintomas por pelo menos alguns anos. Mas, com o tempo, as células crescem e se espalham para outras partes do corpo, incluindo os gânglios linfáticos, fígado e baço.
Leucemia Mieloide Crônica (LMC)
Também conhecida como leucemia mielogênica crônica
É um tipo de câncer que começa em certas células formadoras de sangue da medula óssea. Na LMC, uma mudança genética ocorre em uma versão inicial (imatura) das células mieloides – as células que produzem glóbulos vermelhos, plaquetas e a maioria dos tipos de glóbulos brancos (exceto linfócitos). Essa mudança forma um gene anormal chamado BCR-ABL, que transforma a célula em uma célula LMC. As células leucêmicas crescem e se dividem, acumulando-se na medula óssea e transbordando para o sangue. Com o tempo, as células também podem se estabelecer em outras partes do corpo, incluindo o baço. LMC é uma leucemia de crescimento bastante lento, mas pode se transformar em uma leucemia aguda de crescimento rápido que é difícil de tratar. A LMC ocorre principalmente em adultos, mas muito raramente também ocorre em crianças. Em geral, o tratamento é igual ao dos adultos.
Leucemia Mielomonocítica Crônica (LMMC)
Começa nas células formadoras de sangue na medula óssea e invade o sangue. As células em quase qualquer parte do corpo podem se tornar câncer e podem se espalhar para outras áreas do corpo. Pessoas com LMMC podem ter falta de algumas células sanguíneas, mas o principal problema são os monócitos em excesso, um tipo de glóbulos brancos. (pelo menos 1.000 por mm3). Frequentemente, a contagem de monócitos é muito maior, fazendo com que sua contagem total de leucócitos também fique muito alta.Normalmente, existem algumas células anormais, chamadas blastos, na medula óssea. A quantidade de explosões na LMMC é inferior a 20%.Muitas pessoas com LMMC têm baços aumentados (um órgão que fica logo abaixo da caixa torácica esquerda).Cerca de 15% a 30% das pessoas com LMMC desenvolvem leucemia mieloide aguda (LMA)O DNA dentro das células anormais não tem certas mudanças nos genes chamados BCR / ABL (cromossomo Filadélfia), ou PDGFRA e PDGRFRB. Como a LMMC tem características tanto de síndrome mielodisplásica quanto de neoplasia mieloproliferativa, os especialistas criaram uma nova categoria para ela: neoplasia mielodisplásica / mieloproliferativa (mielo – medula óssea, proliferativa – crescimento excessivo, displásica – aparência anormal). A LMMC é a doença mais comum nesse grupo. Doenças muito menos comuns nesse grupo são a leucemia mieloide crônica atípica e a leucemia mielomonocítica juvenil (LMMJ). Todas essas doenças produzem muitas células sanguíneas anormais. A leucemia mieloide crônica é um exemplo de neoplasia mieloproliferativa em que há uma superprodução de glóbulos brancos do sangue.
Leucemia Infantojuvenil
As leucemias são cânceres que começam nas células que normalmente se desenvolveriam em diferentes tipos de células do sangue. Na maioria das vezes, a leucemia começa nas formas iniciais de glóbulos brancos, mas algumas leucemias começam em outros tipos de células sanguíneas. Existem diferentes tipos de leucemia, que se baseiam principalmente em:
Se a leucemia for aguda (crescimento rápido) ou crônica (crescimento mais lento).
Se a leucemia começar nas células mieloides ou linfoides.
Saber o tipo específico de leucemia que uma criança e/ou adolescente tem pode ajudar os médicos a prever melhor o prognóstico (perspectiva) de cada criança e selecionar o melhor tratamento.
Leucemias Agudas
A maioria das leucemias infantojuvenis são agudas. Essas leucemias podem progredir rapidamente e geralmente precisam ser tratadas imediatamente. Os principais tipos de leucemia aguda são:
Leucemia linfocítica (linfoblástica) aguda (LLA): cerca de 3 em cada 4 leucemias infantojuvenis são LLA. Essas leucemias começam nas primeiras formas de glóbulos brancos do sangue chamadas linfócitos.
Leucemia mieloide aguda (LMA): este tipo de leucemia, também chamada de ou leucemia não linfocítica aguda, é responsável pela maioria dos casos restantes de leucemia infantojuvenil. A LMA começa a partir das células mieloides que normalmente formam os glóbulos brancos (exceto linfócitos), glóbulos vermelhos ou plaquetas.
Raramente, as leucemias agudas podem apresentar características tanto de LLA quanto de LMA. Estas são chamadas de leucemias de linhagem mista, leucemias agudas indiferenciadas ou Leucemias Agudas de Fenótipo Misto.
Leucemia Crônica
As leucemias crônicas são raras em crianças e adolescentes. Essas leucemias tendem a crescer mais lentamente do que as leucemias agudas, mas também são mais difíceis de curar. As leucemias crônicas podem ser divididas em 2 tipos principais:
Leucemia mieloide crônica (LMC): também chamada de leucemia mieloide crônica, a LMA é rara em crianças e adolescentes. O tratamento é semelhante ao usado para adultos.
Leucemia linfocítica crônica (LLC): essa leucemia é extremamente rara em crianças e adolescentes.
Leucemia Mielomonocítica Juvenil (LMMJ)
Este tipo raro de leucemia não é crônica nem aguda. Começa nas células mieloides, mas geralmente não cresce tão rápido quanto a LMA ou tão lentamente quanto a LMC. Ocorre com mais frequência em crianças pequenas (idade média de 2 anos). Os sintomas podem incluir pele pálida, febre, tosse, hematomas ou sangramento fácil, dificuldade para respirar (devido a muitos glóbulos brancos nos pulmões), erupção cutânea e aumento do tamanho do baço, fígado e nódulos linfáticos.
Imagem: National Cancer Institute
- Fatores de Risco
-
Mais informações em breve.
- Sintomas
-
Mais informações em breve.
- Diagnóstico
-
Mais informações em breve.
- Tratamento
-
Mais informações em breve.
- Estadiamento
-
Mais informações em breve.